题目内容
某混有另一种金属粉末的铁粉28克与足量盐酸反应可生成0.9克氢气,则有的这种杂质可能是( )
| A、镁粉 | B、锌粉 | C、铝粉 | D、铜粉 |
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:根据铁与盐酸反应的化学方程式可以计算出28g纯铁能生成1g氢气.由于0.9g<1g,说明不纯的铁中所含的杂质不能与盐酸反应或等质量的铁和所含杂质相比,杂质与盐酸反应产生的氢气少.
解答:解:
铜在金属活动顺序表中排在氢的后面,说明铜不能与盐酸反应;
根据产生氢气的质量=
×金属质量,而镁、锌、铝、铁的化合价分别为+2、+2、+3、+2;而镁、锌、铝、铁的相对原子质量分别:24、65、27、56,因此等质量的镁、铝、锌、铁与盐酸反应时产生的氢气质量由多到少的顺序是:铝>镁>铁>锌.
结合上述分析说明杂质可能为铜或锌.
故选:B、D.
铜在金属活动顺序表中排在氢的后面,说明铜不能与盐酸反应;
根据产生氢气的质量=
| 金属的化合价 |
| 金属的相对原子质量 |
结合上述分析说明杂质可能为铜或锌.
故选:B、D.
点评:本题的关键是所含杂质:根据产生氢气的质量=
×金属质量,进行分析.
| 金属的化合价 |
| 金属的相对原子质量 |

练习册系列答案
相关题目
下列化学方程式书写正确的是( )
| A、CH4+2O2═CO2+2H2O |
| B、NaOH+H2SO4═Na2SO4+H2O |
| C、Fe2O3+6HCl═2FeCl3+3H2O |
| D、H2O2═H2+O2 |
日常生活中用到的下列物质,属于纯净物的是( )
| A、调味用的食醋 |
| B、取暖用的煤 |
| C、速溶葡萄糖 |
| D、炒菜用的铁锅 |
如图所示,实验装置或实验基本操作中,不正确的是( )
A、 |
B、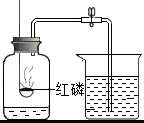 |
C、 |
D、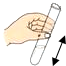 |
下列四种物质中,有一种物质在一定条件下能跟其它三种物质都发生反应.这种物质是( )
| A、CuSO4 |
| B、O2 |
| C、HCl |
| D、Fe |
下列化学方程式书写正确的是( )
A、4Fe+3O2
| ||||
B、2H2+O2
| ||||
| C、Zn+H2SO4═ZnSO4+H2↑ | ||||
D、4P+5O2
|
埋在地下的自来水管道,最适宜的一种管道是( )
| A、镀锌管 | B、硬铝管 |
| C、不锈钢管 | D、铸铁管 |
在天平两端各放置一个盛有等质量、等溶质质量分数的盐酸的烧杯,把天平调至平衡.在左边烧杯中放入3.6克铝粉,为了使天平平衡,在右边的烧杯中应该放入镁粉的质量为( )克.
| A、3.6 | B、3.5 |
| C、3.49 | D、3.7 |