题目内容
15.如图1所示,有人制作了一个家庭制氧装置.该制氧装置由2个饮料瓶、2根软管和药剂构成,整套装置成本不到3块钱.药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过B管从乙瓶导出,即可供人吸氧.
(1)为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应不伸入液面.(选填“不伸入液面”或“伸入液面”)
(2)药剂加入水中后会发生以下两个反应:
2Na2CO3•3H2O2═2Na2CO3+3H2O2;2H2O2═2H2O+O2↑
从化学反应的基本类型来看,它们都属于分解反应.
(3)小红完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物、放入大试管中加热至质量不再变化为止.根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量.(学习小组同学事先查阅资料获知,氯酸钾分解的化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{加热}$2KCl+3O2↑),(二氧化锰的质量在反应前后不变且在水中难溶.)
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图2所示.
请你完成下表:(写出具体计算步骤)
| 反应中产生氧气的质量/克 | 原混合物中氯酸钾的质量/克 | 原混合物中氯酸钾的质量分数 |
| 4.8 | 12.25 | 76.5625% |
分析 根据反应物、生成物的种类可以判断反应类型;
根据反应的化学方程式、图中提供的信息可以进行相关方面的计算和判断.
解答 解:(1)为了顺利地导出甲瓶中产生的氧气,A软管在甲瓶中应不伸入液面.
故填:不伸入液面.
(2)从化学反应的基本类型来看,反应物都是一种,生成物都是两种,它们都属于分解反应.
故填:分解.
(3)设氯酸钾质量为x,
反应生成氧气质量为:16.0g-11.2g=4.8g,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$,
x=12.25g,
原混合物中氯酸钾的质量分数为:$\frac{12.25g}{16.0g}$×100%=76.5625%,
故填:4.8;12.25;76.5625%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
5.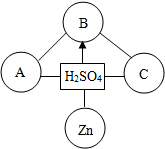 如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
 如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是( )| A. | NaOH、CuSO4、Na2CO3 | B. | Ba(OH)2、CuCl2、CuO | ||
| C. | Cu(OH)2、HCl、Fe2O3 | D. | NaOH、HCl、Na2CO3 |
6.铝在生产生活中的应用非常广泛,如图为铝在元素周期表中的信息,由此不能直接得到的信息是( )
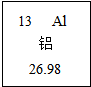

| A. | 铝元素属于金属元素 | B. | 铝元素的原子序数为13 | ||
| C. | 铝元素的相对原子质量为26.98 | D. | 铝元素位于元素周期表中第三周期 |
3.往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是( )
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu、滤液中有Zn2+、Cu2+Fe2+ | |
| D. | 滤纸上有Ag、Cu、Fe、滤液中有Zn2+、Fe2+ |
4.下列各组物质中,都是由分子构成的是( )
| A. | 水、氢气 | B. | 铁、氧气 | C. | 氯化钠、石墨 | D. | 氯化钠、水 |
5.下列是四位同学分别设计的实验方案,你认为可行的是( )
| A. | 某固体中加入稀盐酸产生无色气体,证明该固体一定含有CO32- | |
| B. | 某溶液中增加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42- | |
| C. | 某无色溶液中滴加无色酚酞试液,溶液变成红色,该溶液不一定是碱 | |
| D. | 把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳 |
