题目内容
有一种含水的过氧化氢(双氧水)样品10 g,在二氧化锰的催化作用下,完全分解得到3.2 g氧气,试求该样品中过氧化氢的质量分数。
【解析】
设参与反应的H2O2质量为x,
2H2O2 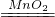 2H2O+O2↑
2H2O+O2↑
68 32
x 3.2g
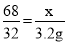
解之得:x=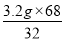 =6.8g ;则该样品中过氧化氢的质量分数为:
=6.8g ;则该样品中过氧化氢的质量分数为: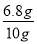 ×100%=68%.
×100%=68%.
答:该样品中过氧化氢的质量分数为68%.
【解析】
试题分析:利用过氧化氢分解的化学方程式和生成氧气的质量,列出比例式,就可计算出该样品中过氧化氢的质量,然后根据质量分数公式计算即可.
考点:根据化学方程式的计算;混合物中某物质的质量分数的计算。

练习册系列答案
相关题目