题目内容
 碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明. 请回答下列问题:
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明. 请回答下列问题:(1)碘酸钾中钾、碘、氧三种元素质量比为
(2)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg.
假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为
考点:标签上标示的物质成分及其含量,元素质量比的计算
专题:标签图示型
分析:(1)根据碘酸钾的化学式(KIO3)可知,碘酸钾中钾、碘、氧三种元素质量比=(钾的相对原子质量×钾原子个数)):(碘的相对原子质量×碘原子个数):(氧的相对原子质量×氧原子个数);
(2)根据“碘元素的质量÷加碘食盐的含碘量”计算即可.
(2)根据“碘元素的质量÷加碘食盐的含碘量”计算即可.
解答:解:
(1)碘酸钾中钾、碘、氧三种元素质量比=39:127:(16×3)=39:127:48;
故答案为:39:127:48;
(2)0.15mg÷20mg∕kg=0.0075kg=7.5g.
故答案为:7.5.
答案:
(1)39:127:48
(2)7.5
(1)碘酸钾中钾、碘、氧三种元素质量比=39:127:(16×3)=39:127:48;
故答案为:39:127:48;
(2)0.15mg÷20mg∕kg=0.0075kg=7.5g.
故答案为:7.5.
答案:
(1)39:127:48
(2)7.5
点评:本题主要考查学生运用化学式进行计算的能力.

练习册系列答案
相关题目
分子和原子的本质区别( )
| A、分子大,原子小 |
| B、分子间有间隔,原子没有 |
| C、分子可以之间构成物质,原子不能 |
| D、在化学变化中,分子可以再分,原子不可分 |
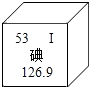 2011年3月11日,日本发生9.0级强地震,福岛电站发生爆炸导致核燃料泄漏.经检测,确认放射性碘扩散到海洋及周围空气中,造成环境污染.如图为元素周期表中碘元素的相关信息,下列说法错误的是( )
2011年3月11日,日本发生9.0级强地震,福岛电站发生爆炸导致核燃料泄漏.经检测,确认放射性碘扩散到海洋及周围空气中,造成环境污染.如图为元素周期表中碘元素的相关信息,下列说法错误的是( )| A、碘元素属于非金属元素 |
| B、碘元素原子的质子数为53 |
| C、碘元素在地壳中的含量为126.9% |
| D、碘元素中一个原子的原子核外有53个电子 |
有A、B、C、D、E、F六种化合物,它们在溶液中可发生如下反应:
(1)B+A→C+H2O; (2)C+KOH→D↓十E (3)E+AgNO3→F(白色)↓+KNO3;
E中加入Ba(NO3)2溶液,无明显现象.则下列判断正确的是( )
(1)B+A→C+H2O; (2)C+KOH→D↓十E (3)E+AgNO3→F(白色)↓+KNO3;
E中加入Ba(NO3)2溶液,无明显现象.则下列判断正确的是( )
| A、B可能是碱性氧化物 |
| B、D不一定是碱 |
| C、F不-定是氯化银 |
| D、B与A的反应一定属于中和反应 |
 如图是某化肥包装袋上的部分说明:
如图是某化肥包装袋上的部分说明: 某同学用如图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
某同学用如图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).