题目内容
5.有一份铁粉与铜粉混合物样品,为了了解其组成,某同学取20g样品加入足量的稀盐酸中,待反应完全后过滤,称得不溶物的质量为6g.试计算:(1)金属混合物中铁的质量分数:
(2)产生氢气的质量.
分析 由于铜在金属活动性顺序中排在氢的后面,不与酸反应,只有铁与硫酸反应,稀硫酸是足量的,所以不溶物为铜的质量,则铁的质量为20g-6g=14g,根据方程式列比例式进行计算,已知量是铁,即可求出氢气的质量.
解答 解:(1)由题意可知,铁的质量为:20g-6g=14g;铁的质量分数=$\frac{14g}{20g}$×100%=70%.
(2)设生成氢气的质量为x
Fe+H2SO4═FeSO4+H2↑
56 2
14g x
$\frac{56}{2}$=$\frac{14g}{x}$
解得:x=0.5g
答:(1)金属混合物中铁的质量是70%;
(2)产生氢气的质量是0.5g.
点评 解答本题的关键是要知道铜与硫酸不反应,因为铜排在了氢的后面,只有排在氢前面的金属才能与酸反应产生氢气.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
7.下列描述属于物质的物理性质的是( )
| A. | 酒精能燃烧 | B. | 铜能导电 | ||
| C. | 氧气具有氧化性 | D. | 二氧化碳能使澄清石灰水变浑浊 |
10.下列基本实验操作的图示不正确的是( )
| A. | 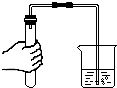 检查装置气密性 | B. | 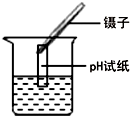 量取液体 量取液体 | C. | 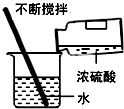 稀释浓硫酸 | D. | 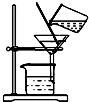 过滤 |
14.下列关于同种元素组成的物质说法错误的是( )
| A. | 可以是单质 | B. | 可以是混合物 | C. | 可以是纯净物 | D. | 可以是化合物 |
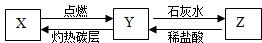 X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如图转化关系.请回答下列问题.
X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如图转化关系.请回答下列问题.