题目内容
19.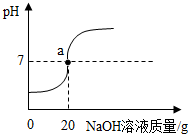 向50g氯化氢和氯化钠的混合溶液中滴加溶质质量分数为20%的氢氧化钠溶液,得到溶液的pH变化曲线如图所示,请回答下列问题:
向50g氯化氢和氯化钠的混合溶液中滴加溶质质量分数为20%的氢氧化钠溶液,得到溶液的pH变化曲线如图所示,请回答下列问题:(1)曲线上a点所表示的意义是盐酸和氢氧化钠恰好完全反应
(2)计算该50%混合溶液中溶质氯化氢的质量.
(3)若已知50%混合溶液中含氯化钠8.15g,则a点所得溶液的溶质质量分数是多少?
分析 (1)根据a点的pH值等于7,说明盐酸和氢氧化钠恰好完全反应进行分析;
(2)根据化学方程式和所用氢氧化钠的质量进行分析;
(3)根据质量守恒定律找出所得溶液的质量,然后计算溶质质量分数.
解答 解:(1)a点的pH值等于7,说明盐酸和氢氧化钠恰好完全反应;
(2)设氯化氢的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
20g×20% x
$\frac{40}{20g×20%}$=$\frac{36.5}{x}$
x=3.65g
(3)所得溶液的溶质质量分数为:$\frac{8.15g}{20g+50g}$×100%=11.6%.
故答案为:(1)盐酸和氢氧化钠恰好完全反应;
(2)3.65g;
(3)11.6%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
9.水是化学实验中常见且用途广泛的一种物质.对下列各实验中水的主要作用的解释不合理的是( )
| A. | 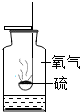 硫在氧气中燃烧--集气瓶好做水:吸收放出的热量 | |
| B. | 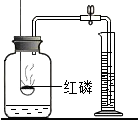 测定空气中氧气含量--量筒中的水:通过水体积变化得到氧气体积 | |
| C. |  细铁丝在氧气中燃烧--集气瓶中的水:防止集气瓶炸裂 | |
| D. | 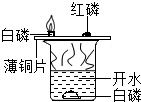 探究燃烧的条件--烧杯中的水:加热铜片:隔绝空气 |
7.下列说法正确的是( )
| A. | 煤、石油和天然气是可再生能源 | |
| B. | 10g氧化钠溶于90g水中得到100g溶液遵循质量守恒定律 | |
| C. | 可燃性气体或粉尘在有限的空间里点燃,有可能引起爆炸 | |
| D. | 一个分子必须由两个以上的原子构成 |
4.通过实验可以获取证据,得出结论.下列做法中不能获得明显证据的是( )
| A. | 为了证明汗水中含有Cl-,加入含稀硝酸的硝酸银溶液 | |
| B. | 为了证明铁粉与硫磺加热后生成新物质,用磁铁靠近生成物 | |
| C. | 为了证明某些金属氧化物可以和水发生反应,把氧化铁粉末放入水中 | |
| D. | 为了证明氢氧化钠固体容易潮解,在表面皿上放置少量氢氧化钠固体暴露在空气中 |
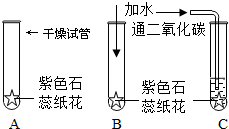 某同学设计了一套验证二氧化碳与水能否反应的实验,他首先用紫色石蕊试纸浸泡滤纸,晒干后折成纸花,然后按如图所示分别进行:
某同学设计了一套验证二氧化碳与水能否反应的实验,他首先用紫色石蕊试纸浸泡滤纸,晒干后折成纸花,然后按如图所示分别进行: