题目内容
11.物质X可发生“X+酸→盐+H2O”的反应,则X可能是( )| A. | Fe | B. | CO2 | C. | H2SO4 | D. | Na2O |
分析 根据酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应),据此进行分析解答.
解答 解:A、铁能与酸反应生成盐和氢气,故选项错误.
B、二氧化碳不能与酸反应,故选项错误.
C、硫酸不能与酸反应,故选项错误.
D、氧化钠属于金属氧化物,能与酸反应生成盐和水,故选项正确.
故选:D.
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
2.某地区土壤的pH值约为5,一些重要作物最适宜生长的土壤pH如下表:
(1)根据上表数据,你认为这种土壤最适合种植的农作物是马铃薯;
(2)若要想种植小麦,你认为最好选用以下②试剂(填序号)来改良土壤;
①氢氧化钠 ②氢氧化钙 ③石灰石
(3)在作物生长过程中需要施用化肥,下列化肥中属于复合肥的是③(填序号).
①NH4HCO3 ②KCl ③KNO3 ④Ca(H2PO4 )2.
| 作物 | 水稻 | 小麦 | 玉米 | 马铃薯 |
| pH | 6-7 | 6.3-7.5 | 6-7 | 4.8-5.5 |
(2)若要想种植小麦,你认为最好选用以下②试剂(填序号)来改良土壤;
①氢氧化钠 ②氢氧化钙 ③石灰石
(3)在作物生长过程中需要施用化肥,下列化肥中属于复合肥的是③(填序号).
①NH4HCO3 ②KCl ③KNO3 ④Ca(H2PO4 )2.
16.下列物质中,属于纯净物的是( )
| A. | 干冰 | B. | 天然气 | C. | 石油 | D. | 大理石 |
3.初三一班的东东人称“小马虎”,下面是从他的笔记中摘录的“微粒符号中对‘2’含义的理解”,你认为正确的是( )
| A. | CO2:“2”表示一个二氧化碳分子含有两个氧原子 | |
| B. | 2Na:“2”表示两个钠元素 | |
| C. | 2H:“2”表示两个氢分子 | |
| D. | Fe2+:“2+”表示铁离子带两个单位正电荷 |
20.为了测定蜡烛中碳、氢两 种元素的质量比,小华设计了如图所示的实验.
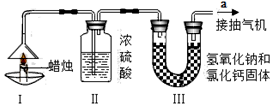
实验步骤如下:
①先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.②按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.③一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如上表.请回答:
①该实验中测得水的质量为1.8g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素质量.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由.
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |

实验步骤如下:
①先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.②按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.③一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如上表.请回答:
①该实验中测得水的质量为1.8g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素质量.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由.
1.马铃薯富含淀粉、蛋白质、维生素C、磷、钙等.下列说法错误的是( )
| A. | 钙元素可以预防佝偻病 | B. | 蛋白质、淀粉属于有机高分子 | ||
| C. | 维生素C可以预防坏血病 | D. | 可用加碘食盐检验马铃薯中的淀粉 |
