题目内容
20.根据下列变化,试推断并写出A、B、C的化学式和②反应的化学方程式
(1)写化学式:AFe BFeSO4 CH2
(2)有关化学方程式:②Fe+CuSO4═FeSO4+Cu.
分析 铁和稀硫酸反应生成硫酸亚铁和氢气,加热条件下氢气和氧化铜反应生成铜和水,铁和硫酸铜反应生成硫酸亚铁和铜.
解答 解:铁和稀硫酸反应生成硫酸亚铁和氢气,加热条件下氢气和氧化铜反应生成铜和水,铁和硫酸铜反应生成硫酸亚铁和铜,因此ABC分别是铁、硫酸亚铁和氢气;
(1)铁的化学式是Fe,硫酸亚铁的化学式是FeSO4,氢气的化学式是H2.
故填:Fe;FeSO4;H2.
(2)铁和硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故填:Fe+CuSO4═FeSO4+Cu.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
12.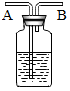 如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
 如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )
如图所示装置有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水.以下说法不正确的是( )| A. | 导管A连接供给氧气的钢瓶 | B. | 导管B连接病人吸氧气的塑胶管 | ||
| C. | 该装置可用来观察输出氧气的速度 | D. | 该装置可用来调节输出氧气的速度 |

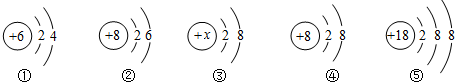
 是氯原子的结构示意图,由此可知,氯原子在化学反应中容易得到电子(选填“得到”或“失去”).
是氯原子的结构示意图,由此可知,氯原子在化学反应中容易得到电子(选填“得到”或“失去”).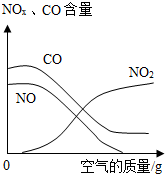 随着人们生活水平的提高和社会的进步,普通老百姓拥有汽车的数量逐年增加,但汽车排放的尾气对大气造成的污染也日趋严重.汽车尾气的化学成份较多,但主要的污染物有CO和NO,其中的NO是空气中的N2和O2在电火花和高温条件下反应生成的,CO是汽油不充分燃烧产生的.
随着人们生活水平的提高和社会的进步,普通老百姓拥有汽车的数量逐年增加,但汽车排放的尾气对大气造成的污染也日趋严重.汽车尾气的化学成份较多,但主要的污染物有CO和NO,其中的NO是空气中的N2和O2在电火花和高温条件下反应生成的,CO是汽油不充分燃烧产生的.