题目内容
【题目】在一烧杯中盛有20gNaCl和Na2CO3组成的固体混合物,加100g水溶解,制成溶液,向其中逐渐滴加溶质质量分数为7.3%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.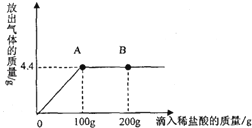
请根据题意回答问题:
(1)当滴加稀盐酸至图中(“A”或“B”)点时,Na2CO3恰好反应完全.
(2)当滴加了100g稀盐酸时,放出气体的总质量为g.
(3)当滴加稀盐酸至图中A点时,烧杯中溶液的总质量为g.
(4)当滴加了100g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量.
【答案】
(1)A
(2)4.4
(3)215.6
(4)
解:设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 4.4g
![]() ,
,
解之得:x=10.6g,y=11.7g,
烧杯里不饱和溶液中溶质的质量为:11.7g+(20g﹣10.6g)=21.1g,
答:其中溶质的质量为21.1g.
【解析】(1)由图示可知,当滴加稀盐酸至图中A点时,气体不再增加,说明碳酸钠已完全反应;故填:A;(2)由图示可知,当滴加了100g稀盐酸时,放出气体的总质量为4.4g.故填:4.4;(3)当滴加稀盐酸至图中A点时,烧杯中溶液的总质量为:20g+100g+100g﹣4.4g=215.6g;故填:215.6;
【考点精析】掌握根据化学反应方程式的计算是解答本题的根本,需要知道各物质间质量比=系数×相对分子质量之比.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目