题目内容
11.将14g生铁放入盛有292g的5%盐酸溶液的烧杯中充分反应,若它们恰好反应,求:(1)反应生成氢气质量是多少?
(2)生铁中铁的质量分数.
(3)反应后的溶液中,氯化亚铁的质量分数.
分析 铁与稀硫酸反应生成硫酸亚铁和氢气,由参加反应的硫酸溶液的质量、溶质的质量分数,由反应的化学方程式,列式计算出生成氢气的质量、参加反应的铁的质量,和生成氯化亚铁的质量即可解答.
解答 解:设生成氢气的质量为X;设生铁中铁的质量为Y;设氯化亚铁的质量为Y
Fe+2HCl=FeCl2+H2↑
56 73 127 2
Y 292g×5% M X
$\frac{56}{Y}=\frac{73}{292g×5%}=\frac{127}{M}=\frac{2}{X}$
(1)X=0.4g
(2)Y=11.2g,
生铁中铁的质量分数:$\frac{11.2g}{14g}×100%$=80%;
(3)M=25.4g
反应后的溶液中,氯化亚铁的质量分数:
$\frac{25.4g}{292g+11.2g-0.4g}×100%$=8.4%
答:(1)生成氢气质量是0.4g,(2)生铁中铁的质量分数是80%;(3)反应后的溶液中FeCl2质量分数8.4%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性

练习册系列答案
相关题目
19.下列实验操作正确的是( )
| A. | 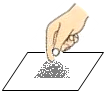 取用氯化钠 | B. |  溶解氯化钠 | C. | 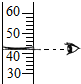 读取水的体积 | D. |  称取氯化钠 |
3.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用①-⑧编号后,做如下实验.下列选项对实验现象的描述错误的是( )


| A. | ①号和⑤号试管中溶液都变红 | B. | ②号和④号试管中都产生气泡 | ||
| C. | ⑦号和⑧号试管中都产生沉淀 | D. | ③号和⑥号试管中溶液都变色 |
20.下列实验现象描述正确的是( )
| A. | 肥皂水滴入硬水中,产生较多的泡沫 | |
| B. | CO2通入无色酚酞试液,溶液变红色 | |
| C. | 红磷在氧气里剧烈燃烧,生成大量白雾 | |
| D. | NH3通入紫色石蕊试液,溶液变蓝色 |
1.下列有关资源、能源的叙述正确的是( )
| A. | 空气是一种宝贵的资源,其中稀有气体的含量为0.03% | |
| B. | 按目前测定,海水中含有的化学物质有80多种 | |
| C. | 煤、石油、沼气、风能等都是可再生能源 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
 ;
;