题目内容
16.验证CO2的相关性质.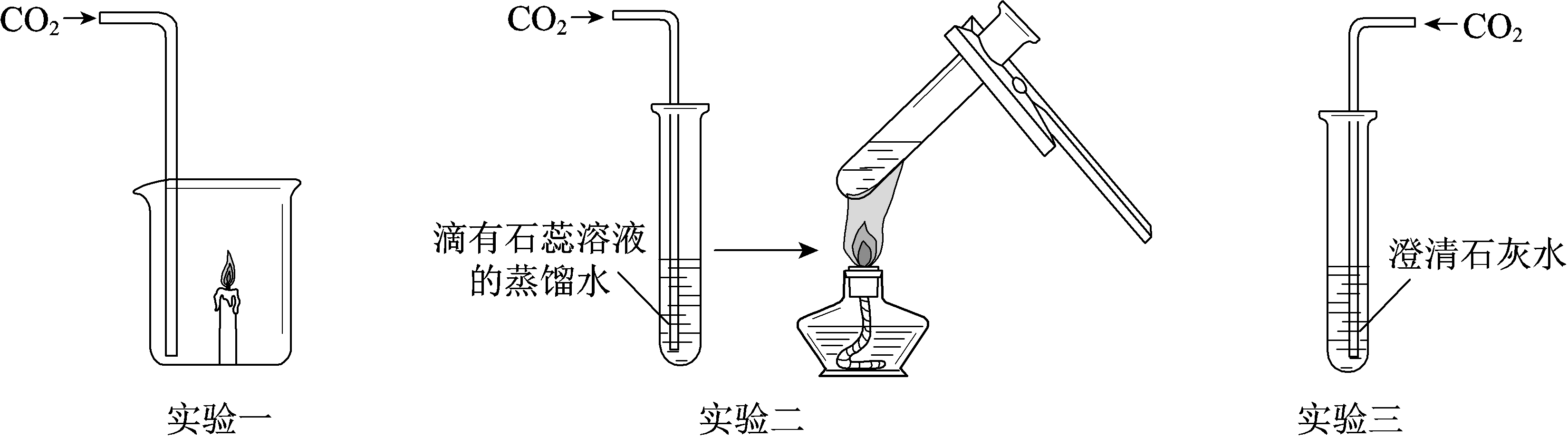
(1)实验一:可证明CO2具有的性质是不燃烧,不支持燃烧,密度比空气大.
(2)实验二:加热液体时可观察到的现象是有气泡产生,液体由红色变为紫色,反应的化学方程式为H2CO3=H2O+CO2↑.
(3)实验三:能证明CO2与石灰水反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据二氧化碳的性质分析回答.二氧化碳不燃烧,不支持燃烧,密度比空气大;能与水化合生成了碳酸,碳酸不稳定易分解;二氧化碳能与氢氧化钙反应生成了碳酸钙和水.
解答 解:(1)实验一:向烧杯中通入二氧化碳,由蜡烛的熄灭,可证明CO2具有的性质是:不燃烧,不支持燃烧,密度比空气大.
(2)实验二:由于碳酸不稳定易分解,所以加热液体时可观察到的现象是:有气泡产生,液体由红色变为紫色,反应的化学方程式为:H2CO3=H2O+CO2↑.
(3)实验三:澄清的石灰水变浑浊,能证明CO2与石灰水反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答为:(1)不燃烧,不支持燃烧,密度比空气大;(2)有气泡产生,液体由红色变为紫色,H2CO3=H2O+CO2↑;(3)CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题的难度不大,了解二氧化碳的性质、方程式的书写是解答本题的基础知识.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
6.下列变化中属于化学变化的是( )
| A. | 冰川融化 | B. | 钢铁生锈 | C. | 汽油挥发 | D. | 海水晒盐 |
7.用燃烧法测定铁合金时,将铁合金置于足量的氧气中燃烧,得到0.44g二氧化碳和29gFe3O4,则铁合金是( )
| A. | 纯铁 | B. | 钢 | C. | 生铁 | D. | 无法判断 |
4.下列项目没有列入空气质量监测的是( )
| A. | N2 | B. | NO2 | C. | SO2 | D. | PM2.5 |
1.下列有关化学实验基本操作的叙述,错误的是( )
| A. | 给试管中药品加热,需先预热 | |
| B. | 制取气体前,需先检查装置的气密性 | |
| C. | 连接乳胶管和玻璃导管,需先用水湿润 | |
| D. | 滴加少量液体时,需将胶头滴管伸入到容器中并紧贴容器内壁 |
8.下列化学用语正确的是( )
| A. | Fe2+:铁离子 | B. | 钠离子结构示意图: | ||
| C. | SO4-2:-2价的硫酸根 | D. | H2:2个氢原子 |
5.草酸(H2C2O4)是生物体的一种代谢产物,广泛分布于植物、动物和真菌体中.下列关于草酸的说法正确的是( )
| A. | 草酸中氢、碳、氧三种元素的质量比为 1:1:2 | |
| B. | 1 个草酸分子中含有 1 个氢分子、2 个碳原子和 2 个氧分子 | |
| C. | 180g 草酸中氧元素的质量是 128g | |
| D. | 草酸中所含碳元素的质量分数为$\frac{12}{1×2+12×2+16×4}$×100% |
6.下列变化中,属于化学变化的是( )
| A. | 酒精挥发 | B. | 海水晒盐 | C. | 湿法冶铜 | D. | 冰雪融化 |