题目内容
19.某化学小组同学为了测定实验室一瓶稀盐酸中溶质的质量分数.他们用铜锌合金和此稀盐酸完成了如图的实验.
请回答:
(1)生成氢气的质量为0.2g.
(2)合金中铜的质量为多少?该瓶稀盐酸中溶质的质量分数为多少?
(3)实验完成后,向烧杯中再加入多少克水,能得到10%的氯化锌溶液?
分析 依据铜锌合金中锌能够和盐酸反应时只有锌能反应而铜不反应,利用质量守恒定律可以求出氢气的质量,利用氢气的质量,根据反应的化学方程式求出参加反应的氯化氢质量,据此分析解答;
解答 解:
(1)依据反应中锌和盐酸反应可以生成氢气,根据质量守恒定律,生成氢气的质量为10g+100g-109.8g=0.2g
设合金中锌额质量为x,参加反应的氯化氢质量为y,生成氯化锌的质量为z
Zn+2HCl═ZnCl2+H2↑
65 73 136 2
x y z 0.2g
$\frac{65}{x}=\frac{73}{y}=\frac{136}{z}=\frac{2}{0.2g}$
x=6.5g y=7.3g z=13.6g
(2)合金中铜的质量为6.5g,该瓶稀盐酸中溶质的质量分数为$\frac{7.3g}{100g}×$100%=7.3%
(3)恰好完全反应后所得溶液质量为:100g+6.5g-0.2g=106.3g
设需加水的质量为m
$\frac{13.6g}{106.3g+m}×$100%=10%
m=29.7g
答案:
(1)0.2g
(2)合金中铜的质量为6.5g 该瓶稀盐酸中溶质的质量分数为7.3%
(3)实验完成后,向烧杯中再加入29.7g水,能得到10%的氯化锌溶液.
点评 本题主要考查学生根据化学方程式进行计算的能力,明确生成氢气的质量和对应的化学反应的关系是解答本题的关键.

练习册系列答案
相关题目
16.正确的设计实验方案时科学探究的重要环节.认真细致的观察和分析实验现象是获得化学知识的重要途径,以下化学实验设计能达到实验目的是( )
| A. | 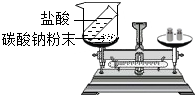 验证质量守恒定律 | B. | 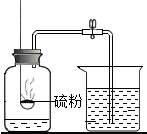 测定空气中的氧气含量 | ||
| C. |  证明CO2密度比空气大 | D. |  证明CO2能与水反应 |
7.青少年处于生长发育期,需要摄取较多的蛋白质.下列食物中蛋白质含量最高的是( )
| A. | 苹果 | B. | 大豆 | C. | 青椒 | D. | 小麦 |
4.下列物质能够导电的是( )
| A. | 固体食盐 | B. | 澄清石灰水 | C. | 糖水 | D. | 蒸馏水 |
8.下列现象能用质量守恒定律解释的是( )
| A. | 水结冰产后质量不变 | |
| B. | 铜粉加热后质量增加了 | |
| C. | 加压降温下氧气变为蓝色液体 | |
| D. | 1升水和1升酒精混合总体积小于2升 |
