题目内容
16.有一氢氧化钠样品,经测定其成分为H2O、Na2CO3和NaOH.取一定质量的此样品,将其加入到盛有200g7.3%盐酸的烧杯中充分反应,再向烧杯中滴加40g10%的NaOH溶液至恰好完全中和,最后将所得溶液蒸干,得到固体的质量是( )| A. | 5.85g | B. | 11.7g | C. | 23.4g | D. | 无法计算 |
分析 根据碳酸钠和盐酸反应生成氯化钠和水、二氧化碳,氢氧化钠和盐酸反应生成氯化钠和水,所以依据氯离子守恒可知,最后得到的固体是氯化钠,依据盐酸和氯化钠之间的关系式进行计算.
解答 解:根据质量守恒定律,氯化钠中所含的氯元素都来自盐酸,而消耗的盐酸的质量为:200g×7.3%=14.6g,
设生成氯化钠的质量为x
HCl----NaCl
36.5 58.5
14.6g x
$\frac{36.5}{14.6g}$=$\frac{58.5}{x}$
x=23.4g
故选:C.
点评 熟练掌握碳酸钠、氢氧化钠与盐酸的反应,知道它们反应生成的盐均为氯化钠,要求氯化钠的质量,可以巧妙的利用质量守恒定律,化学反应前后氯元素的质量不变,找出盐酸和氯化钠的质量关系进而完成解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.水是生命之源,也是重要的溶剂.下列说法不正确的是( )
| A. | 水通电生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| B. | 生活中,我们可以用肥皂水来区分硬水和软水 | |
| C. | 生石灰能用做食品干燥剂,是因为生石灰与水反应而除去水 | |
| D. | 河水经沉降、过滤、吸附、灭菌等净化操作后,得到的水仍为混合物 |
7.如表所示事实的微观解释错误的是( )
| 选项 | 事实 | 微观解释 |
| A | 温度降低,汽油的密度增大 | 分子的体积变小 |
| B | 春天公园里散发出阵阵花香 | 分子在不断运动 |
| C | 氯化钠的水溶液可以导电 | 有自由移动的离子 |
| D | 水在通电条件下生成氢气和氧气 | 氢、氧原子重新组合 |
| A. | A | B. | B | C. | C | D. | D |
4.下列社会活动中,符合节约、节能、减排、防污的是( )
| A. |  大办酒席 | B. |  鲜花扫墓 | C. |  工业排污 | D. |  燃放爆竹 |
11.化学式一门以实验为基础的科学,正确的实验操作是保证进行化学实验成功的重要保障,以下操作中合理的是( )
| A. | 将pH试纸润湿后再测定溶液的酸碱度 | |
| B. | 称量氢氧化钠时,将其放在托盘天平的左盘的纸上 | |
| C. | 检验二氧化碳是否集满时,将燃着的木条伸入集气瓶底 | |
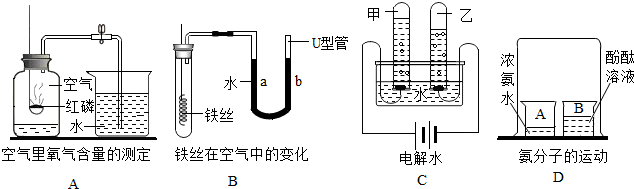
| D. | 做铁丝在氧气燃烧实验时,预先在集气瓶中加少量的水 |
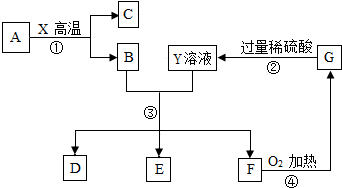 A、B、C、D、E、F、G、X为常见的物质,其中C、D、F属于单质,A、F是红色固体,D、X是无色气体,它们之间的相互转化关系如下图所示,反应①是炼铁工业中的主要反应.
A、B、C、D、E、F、G、X为常见的物质,其中C、D、F属于单质,A、F是红色固体,D、X是无色气体,它们之间的相互转化关系如下图所示,反应①是炼铁工业中的主要反应. 有A、B、C、D四种可溶性化合物,分别由Ag+、Mg2+、Ba2+、Fe3+、Cl-、SO42-、NO3-、OH-八种离子中的一种阳离子和一种阴离子构成(每种离子只能选用一次).将A、B、C、D的溶液两两混合,发生的现象为:
有A、B、C、D四种可溶性化合物,分别由Ag+、Mg2+、Ba2+、Fe3+、Cl-、SO42-、NO3-、OH-八种离子中的一种阳离子和一种阴离子构成(每种离子只能选用一次).将A、B、C、D的溶液两两混合,发生的现象为: