题目内容
8.一包白色粉末由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH、Mg(OH)2、KNO3中的几种混合而成.为探究其组成,进行以下实验:①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀,上层清液为无色.
②过滤,得到白色沉淀A及无色滤液,并将无色滤液分成均匀两份.
③测得其中一份滤液的pH大于7,在另一份滤液中通入二氧化碳气体,产生白色沉淀.
④取干燥的白色沉淀15克,加入足量稀盐酸,白色沉淀全部溶解,且产生无色气体产生5.5克.
据此推断,该白色粉末中一定含有CaCO3、BaCl2、NaOH、Mg(OH)2,可能含有KNO3,一定不含有CuSO4、Na2SO4.
分析 根据硫酸铜溶于水得到蓝色溶液,而本题中得到是无色的溶液,所以在混合物中一定不含硫酸铜,同时能形成白色沉淀的为碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀硝酸,所以沉淀A为碳酸钙,即硫酸钠可以氯化钡最多含有一种,根据“取干燥的白色沉淀15克,加入足量稀盐酸,白色沉淀全部溶解,且产生无色气体产生5.5克”,则推测沉淀为碳酸钙、氢氧化镁,然后结合题中的现象分析判断并解答该题.
解答 解:硫酸铜溶于水得到蓝色溶液,而本题中得到是无色的溶液,所以在混合物中一定不含硫酸铜,同时能形成白色沉淀的为碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀硝酸,所以沉淀B为碳酸钙,即硫酸钠可以氯化钡最多含有一种,向无色滤液C中通入一定量二氧化碳,产生白色沉淀D,所以粉末中含有氢氧化钠,氢氧化钠和二氧化碳反应生成碳酸钠,碳酸钠和氯化钡生成碳酸钡沉淀,粉末中含有氯化钡,不含硫酸钠;根据“取干燥的白色沉淀15克,加入足量稀盐酸,白色沉淀全部溶解,且产生无色气体产生5.5克”,则推测沉淀为碳酸钙、氢氧化镁,综合分析,原白色粉末中一定含有:CaCO3、BaCl2、NaOH、Mg(OH)2,可能含有KNO3,一定不含:CuSO4、Na2SO4.
故答案为:
CaCO3、BaCl2、NaOH、Mg(OH)2;KNO3;CuSO4、Na2SO4.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
19.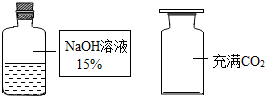 氢氧化钠是一种常用的试剂,在实验课上,同学们对氢氧化钠的性质进行了探究,请你参与他们的活动并回答下列问题
氢氧化钠是一种常用的试剂,在实验课上,同学们对氢氧化钠的性质进行了探究,请你参与他们的活动并回答下列问题
【提出问题】将二氧化碳通入氢氧化钠溶液中看不到任何现象,氢氧化钠与二氧化碳是否发生了反应
【设计方案】小林同学用如图所示的实验仪器与药品以及下列实验操作步骤进行探究.请你预测有关化学反应,写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O,将预测的实验现象以及产生此现象的原因填入如表:
【质疑评价】小芳指出以上实验不足以证明氢氧化钠与二氧化碳气体确实发生了反应,她这样分析的原因是二氧化碳能与水反应.
在小林实验的基础上,请你自选药品帮助他设计一个补充实验,证明氢氧化钠与二氧化碳气体确实发生了反应(写出实验步骤、实验现象)取同样的两个矿泉水瓶,充满二氧化碳气体,加入同体积的水和氢氧化钠溶液,观察到加入氢氧化钠溶液的矿泉水瓶变瘪的明显.
 氢氧化钠是一种常用的试剂,在实验课上,同学们对氢氧化钠的性质进行了探究,请你参与他们的活动并回答下列问题
氢氧化钠是一种常用的试剂,在实验课上,同学们对氢氧化钠的性质进行了探究,请你参与他们的活动并回答下列问题【提出问题】将二氧化碳通入氢氧化钠溶液中看不到任何现象,氢氧化钠与二氧化碳是否发生了反应
【设计方案】小林同学用如图所示的实验仪器与药品以及下列实验操作步骤进行探究.请你预测有关化学反应,写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O,将预测的实验现象以及产生此现象的原因填入如表:
| 实验步骤 | 预测实验现象 | 产生此现象的原因 |
| 向集气瓶中倒入少量的氢氧化钠溶液,立即盖好玻璃片,振荡,将集气瓶倒置,把扶在玻璃片上的手移开 | 玻璃会吸在集气瓶口 | 氢氧化钠与二氧化碳反应,导致瓶内的气压减小 |
在小林实验的基础上,请你自选药品帮助他设计一个补充实验,证明氢氧化钠与二氧化碳气体确实发生了反应(写出实验步骤、实验现象)取同样的两个矿泉水瓶,充满二氧化碳气体,加入同体积的水和氢氧化钠溶液,观察到加入氢氧化钠溶液的矿泉水瓶变瘪的明显.
16.下列实验不能达到目的是( )
| A. | 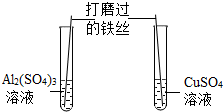 探究铝、铁、铜的金属活动性顺序 | B. | 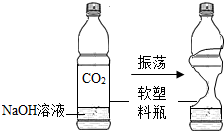 验证二氧化碳与氢氧化钠反应 | ||
| C. | 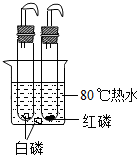 探究燃烧的条件 | D. | 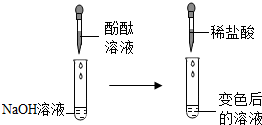 验证氢氧化钠与盐酸反应 |
3.下列转化能一步完成的是( )
①CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④Ba(OH)2→NaOH ⑤CuO→Cu.
①CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④Ba(OH)2→NaOH ⑤CuO→Cu.
| A. | ①③④⑤ | B. | ①②③④⑤ | C. | 只有①③④ | D. | 只有①③⑤ |
13.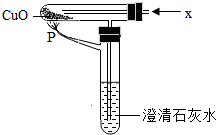 在如图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰石变浑浊,则X可以是( )
在如图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰石变浑浊,则X可以是( )
 在如图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰石变浑浊,则X可以是( )
在如图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰石变浑浊,则X可以是( )| A. | H2 | B. | O2 | C. | CO | D. | CO2 |
20.一些物质在常温下的近似pH如下表:
下列有关上述四种物质的说法中正确的是( )
| 物质 | 血浆 | 胃液 | 正常雨水 | 葡萄汁 |
| PH | 7.35~7.45 | 0.9~1.5 | 5.6 | 3.5~4.5 |
| A. | 只有血浆显碱性 | B. | 只有葡萄汁显酸性 | ||
| C. | 正常雨水显中性 | D. | 胃酸过多的人应多饮用葡萄汁 |
1.下列实验现象的描述中,正确的是( )
| A. | 木炭在氧气中燃烧,发出白光,放出热量 | |
| B. | 木炭在氧气中燃烧更旺,火焰呈明亮的蓝紫色,生成有刺激性气味的气体 | |
| C. | 铁在氧气中燃烧更旺,发出白光,产生大量的白烟,放出热量 | |
| D. | 铁在氧气中剧烈燃烧,火星四射,生成氧化铁,放出热量 |