题目内容
1. 某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:①称取x g胆矾晶体,研细后加入10mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | / | |
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)上述实验步骤中需要使用玻璃棒的是①②③(填序号).
(2)表格中的“待测数据”是指生成50mL气体所需要的时间.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意ad(填字母编号).
a.视线与凹液面最低处相平
b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1mL,刻度A为19,则此时气体的读数为19.8.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 1往KClO3中加入CuO后加热并与未加CuO时进行比较 2固体冷却后溶解、过滤、洗涤、烘干、称量 3将称量后的固体与H2或CO反应 | 检验CuO能否加快KClO3的分解 检查反应前后CuO的质量是否发生了改变 检查反应后CuO的化学性质是否发生了改变 |
分析 本探究题的目的是证明氧化铜对氯酸钾的催化作用,过程是先用胆矾通过化学方法制取氧化铜,再让氧化铜与氯酸钾混合加热,并与二氧化锰与氯酸钾混合加热比较生成等量氧气所需的时间,来证明氧化铜对氯酸钾分解也具有催化作用.由于①②③步中有溶解,过滤,转移固体等操作,所以都要用的玻璃棒,表格中的“待测数据”应是本实验的关键,就是测定反应时间,读取反应前后量气管中液面的读数要准确,方法要规范,如果要进一步探究CuO在反应中是否起到催化作用时,要从催化剂的特点入手,即反应前后催化剂的质量和化学性质都不改变.
解答 解:(1)由于①②③步中有溶解,过滤,转移固体等操作,所以都要用的是玻璃棒.
(2)本题的目的是验证氧化铜的催化作用,关键是测定反应时间,所以表格中的“待测数据”就是测定反应时间,
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,视线与凹液面最低处相平,读数前应上下移动水准管,待两管液面相平再读数.
(4)注意量气管的刻度是上面小,下面大,所以读数应是19.8mL.
(5)如果要进一步探究CuO在反应中是否起到催化作用,要从催化剂的特点入手,通过实验来验证反应前后催化剂的质量和化学性质都不改变.
答案:(1)①②③;
(2)生成50mL气体所需要的时间;
(3)ad;
(4)19.8;
(5)
| 实验步骤 | 设计这一步骤的目的 |
| 1往KClO3中加入CuO后加热并与未加CuO时进行比较 2固体冷却后溶解、过滤、洗涤、烘干、称量 3将称量后的固体与H2或CO反应 | 检验CuO能否加快KClO3的分解 检查反应前后CuO的质量是否发生了改变 检查反应后CuO的化学性质是否发生了改变 |
点评 认真阅读题干是解决这类题的基础,明确题目要求,读懂出题者要考查的意图,逐一分析,才能得出正确答案.

练习册系列答案
相关题目
11.“西气东输”工程是我国一项重大工程,主要把西部的天然气输送到发达的东部地区,既调整能源结构又发展了清洁能源,这些天然气的主要成分是( )
| A. | 氢气 | B. | 一氧化碳 | C. | 甲烷 | D. | 氧气 |
12.今年,华北地区多次雾霾红色预警,雾霾天气会引发呼吸系统疾病,主要原因是空气中PM2.5含量升高.PM2.5是指大气中直径小于或等于2.5微米的颗粒物.下列情况通常不可能引起大气中PM2.5增大的是( )
| A. | 焚烧秸杆 | B. | 光合作用 | C. | 燃烧煤炭 | D. | 汽车尾气 |
6.下列关于金属有关的说法正确的是( )
| A. | 生铁和钢都是铁的合金 | |
| B. | 银的导电性比铜强,所以一般用银作导线 | |
| C. | 铁矿石在地壳中含量最丰富,可以随意开采 | |
| D. | 铝不易被腐蚀,是因为铝的活泼性差 |
12.如表所示的表格中列出了硝酸钾在不同温度下的溶解度:
(1)从表中能得到什么信息:硝酸钾的溶解度随着温度的升高逐渐增大.
(2)20℃时,将15克硝酸钾放入50克水中,充分溶解,得到的溶液是不饱和(填饱和或不饱和)溶液,若20克硝酸钾放入50克水中,所得溶液中溶质的质量分数13%.
| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(克) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,将15克硝酸钾放入50克水中,充分溶解,得到的溶液是不饱和(填饱和或不饱和)溶液,若20克硝酸钾放入50克水中,所得溶液中溶质的质量分数13%.

 某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.
某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.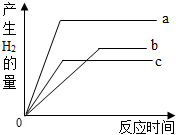 图是a、b、c三种金属在相同条件下与相同浓度的盐酸反应的图象,试回答:
图是a、b、c三种金属在相同条件下与相同浓度的盐酸反应的图象,试回答: