题目内容
2.将一定质量的铁粉放入AgNO3与Zn(NO3)2的混合溶液中,充分反应后,过滤,向滤液、滤渣中滴入稀盐酸,均无明显现象.则下列对滤渣和滤液的成分判断中,不正确的是( )| A. | 滤液中一定有3种金属阳离子 | B. | 滤液颜色一定为浅绿色 | ||
| C. | 滤渣中一定只含有单质银 | D. | 滤渣中一定不含锌、铁 |
分析 锌比铁活泼,铁比银活泼,将一定质量的铁粉放入AgNO3与Zn(NO3)2的混合溶液中,铁不能和硝酸锌反应,能和硝酸银反应生成硝酸亚铁和银;
稀盐酸和铁反应生成氯化亚铁和氢气,和硝酸银反应生成白色沉淀氯化银和硝酸.
解答 解:将一定质量的铁粉放入AgNO3与Zn(NO3)2的混合溶液中,充分反应后,过滤,向滤液、滤渣中滴入稀盐酸,均无明显现象,说明铁和硝酸银恰好完全反应;
A、滤液中有2种金属阳离子,分别是亚铁离子和锌离子,该选项说法不正确;
B、滤液中含有硝酸亚铁和硝酸锌,因此溶液颜色一定为浅绿色,该选项说法正确;
C、铁和硝酸银恰好完全反应,因此滤渣中一定只含有单质银,该选项说法正确;
D、滤渣中一定不含锌、铁,该选项说法正确.
故选:A.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
12.今冬持续多天,遇布大半个中国的雾霾天气把环保问题提到了前所未有的关注高度.下列做法不利于有效治理雾霾天气的是( )
| A. | 将农业上的秸杆粉碎后就地还田 | |
| B. | 电厂、水泥厂远离城市排放含PM2.5的烟尘 | |
| C. | 优化建筑设计,增强室内自然采光,减少照明用电 | |
| D. | 提倡乘公交或骑自行车出行,减少私家车的使用时间 |
13.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | KNO3 HCl CaCl2 | B. | NaCl BaCl2 Na2CO3 | ||
| C. | H2SO4 FeCl3 NaNO3 | D. | NaOH HNO3 NH4NO3 |
10.实验操作是科学的核心技能.下列图示的实验操作中,正确的是( )
| A. | 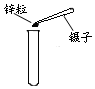 向试管中加锌粒 | B. | 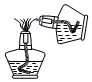 点燃另一酒精灯 | ||
| C. | 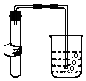 检查装置的气密性 | D. | 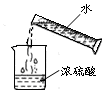 稀释浓硫酸 |
17.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )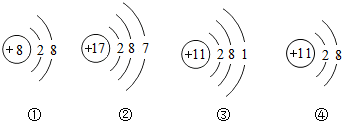

| A. | ①带负电荷 | B. | ②易形成阳离子 | C. | ③④属于同种元素 | D. | ④化学性质稳定 |
14.给某种蔬菜施含放射性同位素15N的氮肥,植物吸收后主要用于合成蛋白质.人食用该蔬菜后,通过新陈代谢,15N最终出现在( )
| A. | 蛋白质中 | B. | 脂肪中 | C. | 氨基酸中 | D. | 尿素中 |
11.利用下列实验器材,能正确完成相应实验的一项是( )
| 选项 | 实验器材 | 相应实验 |
| A | 烧杯、普通漏斗、滤纸、铁架台 | 过滤粗食盐 |
| B | 木板、小桌、砝码 | 影响压力作用效果的因素 |
| C | 相同斜面、不同粗糙程度的水平木板,相同小车 | 研究阻力对物体运动的影响 |
| D | 烧杯、pH试纸、标准比色卡、玻璃片 | 测雨水酸碱度 |
| A. | A | B. | B | C. | C | D. | D |
12.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 碘 | B. | 植物油 | C. | 食盐 | D. | 硫酸钡 |