题目内容
已知某原子的相对原子质量为23,核内中子数为12,则核电荷数为 ,该原子的符号为 .
| 原子的有关数量计算;元素的符号及其意义.. | |
| 专题: | 物质的微观构成与物质的宏观组成. |
| 分析: | 根据在原子中质子数=核电荷数=核外电子数=原子序数,以及相对原子质量≈质子数+中子数判断. |
| 解答: | 解:已知某原子的相对原子质量为23,核内中子数为12,依据相对原子质量=质子数+中子数,可知该原子的质子数为23﹣12=11,该原子是钠原子.根据在原子中,质子数=核电荷数,则质子数=核电荷数=11; 故填:11;Na. |
| 点评: | 本题考查学生对在原子中,原子序数=质子数=核电荷数=核外电子数,相对原子质量=质子数+中子数理解与在解题中应用的能力. |

下列解释不正确的是 ( )
| 事 实 | 解 释 |
| A.H2O2可杀菌消毒,而H2O不能 | 两种物质的分子构成和性质 |
| B.温度计中的水银(汞)热胀冷缩 | 原子的大小发生改变 |
| C.气体易被压缩 | 气体分子间的间隔很大 |
| D.花香四溢 | 分子在不断运动 |
下列反应既属于氧化反应又属于化合反应的是( )
|
| A. | 碳酸→二氧化碳+水 | B. | 氯化氢+氨气→氯化铵 |
|
| C. | 硫+氧气 | D. | 石蜡+氧气 |
2013年12月2日,嫦娥三号月球探测器发射成功,使中国成为第三个掌握月球软着陆和月面巡视探测技术的国家.在飞船的火箭推进器中常装有液态肼(用X表示)和过氧化氢(H2O2),它们混合时的反应方程式为:2H2O2+X=N2↑+4H2O,X的化学式为( )
|
| A. | N2H6 | B. | N2H4 | C. | NH2 | D. | N2H4O2 |
二甲醚(CH3OCH3)可由一氧化碳和物质X在一定的条件下制得.反应的化学方程式为2CO+4X═CH3OCH3+H2O,则X的化学式为( )
|
| A. | H2 | B. | H2O2 | C. | C2H4 | D. | C2H5OH |
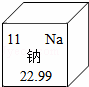
元素周期表中钠元素的信息如图所示,对图中信息理解不正确的是( )
|
| A. | 质子数为11 | B. | 元素名称为钠 |
|
| C. | 元素符号为Na | D. | 核外电子数为22.99 |
 不同
不同 二氧化硫
二氧化硫