题目内容
10. 用如图装置完成以下实验:
用如图装置完成以下实验:(1)探究燃烧条件,若B处盛放 木炭:
I.先在A处通入氮气一段时间,在B处加热,B、C处没有明显变化
II.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
III.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊.
I与III对比,说明燃烧的条件之一是氧气,II与III对比.说明燃烧,的条件之一是温度达到着火点
(2)模拟工业炼铁:若B处盛放氧化铁粉末.在A处通入一氧化碳一段时间后,B处下方用喷灯加热,B处可观察到的现象为固体由红色变为黑色.尾气处理的方法为将酒精灯放于导管口点燃尾气;《自然》杂志刊栽“绿色炼铁”技术;电解熔融的氧化铁得到铁和氧气,该反应的化学方程式:2Fe2O3$\frac{\underline{\;通电\;}}{\;}$4Fe+3O2↑.该炼铁技术另一种产物的用途为供给呼吸.
分析 (1)根据控制变量法的具体操作进行分析;
(2)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,一氧化碳有毒,熔融的氧化铁在通电的条件下生成铁和氧气,氧气能供给呼吸进行分析.
解答 解:(1)Ⅰ与Ⅲ对比,通入的气体不同,温度相同,所以说明燃烧的条件之一是:氧气;
Ⅱ与Ⅲ对比,通入的气体相同,温度不同,所以说明燃烧的条件之一是:温度达到着火点;
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,所以B处可观察到的现象为固体由红色变为黑色,一氧化碳有毒,所以尾气处理的方法为:将酒精灯放于导管口点燃尾气,熔融的氧化铁在通电的条件下生成铁和氧气,化学方程式为:2Fe2O3$\frac{\underline{\;通电\;}}{\;}$4Fe+3O2↑,氧气能供给呼吸、支持燃烧等.
故答案为(1)氧气,温度达到着火点;
(2)固体由红色变为黑色,将酒精灯放于导管口点燃尾气,2Fe2O3$\frac{\underline{\;通电\;}}{\;}$4Fe+3O2↑,供给呼吸(答案合理即可).
点评 本题主要考查了燃烧条件的探究和工业炼铁原理的相关知识,难度不大,需要加强基础知识的记忆即可解答.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
20.下列物质不能鉴别盐酸和氢氧化钠溶液的是( )
| A. | 紫色石蕊试剂 | B. | PH试纸 | C. | 铁粉 | D. | 氯化钠溶液 |
18.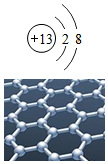 已知某微粒的结构示意图如图所示,下列说法不正确的是( )
已知某微粒的结构示意图如图所示,下列说法不正确的是( )
 已知某微粒的结构示意图如图所示,下列说法不正确的是( )
已知某微粒的结构示意图如图所示,下列说法不正确的是( )| A. | 该微粒具有相对稳定结构 | |
| B. | 该微粒表示的是阳离子 | |
| C. | 该元素属于金属元素 | |
| D. | 该元素位于元素周期表中的第二周期 |
15.在校运会上,50m短跑的运动场上发令抢打响后,产生的白烟主要是( )
| A. | 二氧化硫 | B. | 水蒸气 | C. | 五氧化二磷 | D. | 二氧化碳 |
2.某兴趣小组在探究物质燃烧的条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿熄灭了.它为什么会熄灭呢?每个人提出了不同的猜想.
【提出猜想】

大家讨论后很难达成一致,于是设计了如下所示的实验装置,并进行实验来验证.
【实验设计及验证】
【实验反思】实验结束后,锥形瓶底部的固体中一定含有的成分是Ca(OH)2、CaCO3、P2O5.
【提出猜想】

大家讨论后很难达成一致,于是设计了如下所示的实验装置,并进行实验来验证.
【实验设计及验证】
| 实验步骤 | 实验现象 | 实验分析 | 实验结论 |
(1)取一小块白磷(着火点为40℃),放在一铝箔制的小盒中,然后放入装有生石灰的锥形瓶内.点燃蜡烛,观察现象 | 燃烧的蜡烛一会儿就熄灭了 | 磷燃烧需满足的条件: ①温度达到着火点; ②与氧气接触 | 猜想正确 的同学是 乙. |
| (2)待冷却后,打开分液漏斗活塞,向锥形瓶中注入少量水,立即关闭活塞,观察现象 | 铝盒中的白磷燃烧,放出热量的同时产生了 大量白烟 |
19.钛(Ti)是一种重要的航天金属材料.我校九年级科学兴趣小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
[提出假设]:①Ti金属活动性比Al强;②Al金属活动性比Cu强.
[查阅资料]:钛能与盐酸反应.
[实验设计]:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量的稀盐酸中反应,观察现象.
[操作分析]:三种金属加入稀盐酸前都先用砂布将表面擦光亮,其目的是A.(只有一个正确答案)
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使反应金属温度相同,易反应
[实验现象]:
[实验结论]:(1)原假设中①不正确(填“①”或“②”)
(2)三种金属的金属活动性由弱至强顺序为Al>Ti>Cu(用化学符号表示).
[结论应用]:能否用铝制容器来盛装波尔多液否(填“能”或“否”).
[提出假设]:①Ti金属活动性比Al强;②Al金属活动性比Cu强.
[查阅资料]:钛能与盐酸反应.
[实验设计]:同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量的稀盐酸中反应,观察现象.
[操作分析]:三种金属加入稀盐酸前都先用砂布将表面擦光亮,其目的是A.(只有一个正确答案)
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使反应金属温度相同,易反应
[实验现象]:
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(2)三种金属的金属活动性由弱至强顺序为Al>Ti>Cu(用化学符号表示).
[结论应用]:能否用铝制容器来盛装波尔多液否(填“能”或“否”).
20.下列各组物质中,前者属于纯净物,后者属于混合物的是( )
| A. | 二氧化碳,五氧化二磷 | |
| B. | 冰水混合物,高锰酸钾分解后的剩余固体 | |
| C. | 矿泉水,澄清石灰水 | |
| D. | 净化后的空气,受污染的空气 |
