题目内容
2.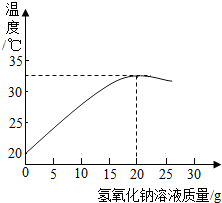 如图表示某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况,查阅资料可知,氢氧化钠和盐酸反应会放出热量.
如图表示某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况,查阅资料可知,氢氧化钠和盐酸反应会放出热量.(1)根据曲线判断,当加入氢氧化钠溶液的质量为20g时,反应恰好完全进行.
(2)当加入15g氢氧化钠溶液时,所得溶液中的溶质为HCl、NaCl(写化学式).
(3)试计算该稀盐酸中溶质的质量分数.
分析 稀盐酸和氢氧化钠反应生成氯化钠和水,当温度达到最高时恰好完全反应,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)根据曲线判断,当加入氢氧化钠溶液的质量为20g时温度最高,反应恰好完全进行.
故填:20g.
(2)当加入15g氢氧化钠溶液时,稀盐酸过量,所得溶液中的溶质为HCl、NaCl.
故填:HCl、NaCl.
(3)设稀盐酸中氯化氢质量为x,
NaOH+HCl═NaCl+H2O,
40 36.5
20g×8% x
$\frac{40}{20g×8%}$=$\frac{36.5}{x}$,
x=1.46g,
该稀盐酸中溶质的质量分数为:$\frac{1.46g}{20g}$×100%=7.3%,
答:该稀盐酸中溶质的质量分数是7.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
18.下列成语蕴含的变化属于化学变化的是.( )
| A. | 刻舟求剑 | B. | 滴水成冰 | C. | 死灰复燃 | D. | 花香四溢 |
10.食品安全重于泰山,下列认识符合科学的是( )
| A. | 用硫酸熏蒸银耳使其雪白光鲜好看 | |
| B. | 食品中添加大量防腐剂以延长其保质期 | |
| C. | 奶茶中加入塑化剂使其口感更香醇 | |
| D. | 食用“加铁酱油”有利于预防缺铁性贫血 |
17.证据是科学探究中获得结论的重要的依据.让我们一起经历一次寻找证据的旅程吧.
【实验目的】制取纯净的硫酸钡(反应原理:Na2SO4+BaCl2═BaSO4↓+2NaCl)
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
(3)如果实验证明氯化钡已经反应完全,要寻找硫酸钡已纯净的证据,我们可以从证明实
验制得的硫酸钡中没有氯化钠(填具体物质)来设计实验方案.
【实验目的】制取纯净的硫酸钡(反应原理:Na2SO4+BaCl2═BaSO4↓+2NaCl)
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已 完全反应 | 取少量滤液,加入稀硫酸 溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已 完全反应 | 无白色沉淀生成 | 硫酸钠未完全反应 |
验制得的硫酸钡中没有氯化钠(填具体物质)来设计实验方案.
7.下列实验操作正确的是( )
| A. | 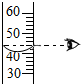 量取液体 | B. | 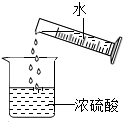 稀释浓硫酸 | C. | 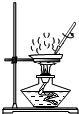 蒸发食盐水 | D. | 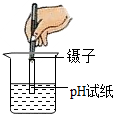 测溶液pH |
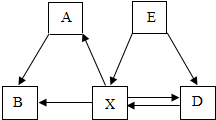 初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无
初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无