题目内容
14.国际上推广使用中国铁锅,这是因为铁锅( )| A. | 是单质 | B. | 含碳,属于混合物 | ||
| C. | 化学性质活泼 | D. | 含人体所需的铁元素 |
分析 根据铁锅的制作原料、铁的生理功能,进行分析判断.
解答 解:中国铁锅是用铁合金制成的,会使被加工的食品中含有铁元素,铁是合成血红蛋白的主要元素,缺乏会患贫血,国际上推广使用中国铁锅,主要是因为铁锅使被加工的食品中含有铁元素,预防缺铁性贫血.
故选:D.
点评 本题难度不大,了解金属的性质与用途、常见金属元素的生理功能与摄入方法等是正确解答本题的关键.

练习册系列答案
相关题目
4.已知反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,其反应类型属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 非基本反应类型 |
9.如图为三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
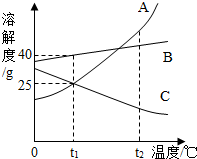

| A. | t1℃时,B物质的溶解度为40g | |
| B. | t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C | |
| C. | 要将C的不饱和溶液转化为饱和溶液可以采取降温的方法 | |
| D. | 要使A从其热饱和溶液中析出,可采用冷却溶液法 |
19.如图实验主要发生化学变化的是( )
| A. |  面粉爆炸 | B. |  洗洁精洗碗 | ||
| C. |  稀释浓硫酸 | D. |  氢气吹肥皂泡 |
6.某课外活动小组通过实践调查得到下列一些结论,你认为其中不科学的是( )
| A. | 使用可降解塑料代替传统塑料,有利于减轻“白色污染” | |
| B. | 稀土是储量较少、不可再生的金属资源 | |
| C. | 一种元素在同一化合物可以显示不同的化合价 | |
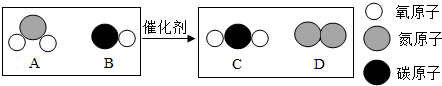
| D. | 催化剂能改变化学反应的速率,而本身的质量和性质在化学反应前后都不会改变 |
3.红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
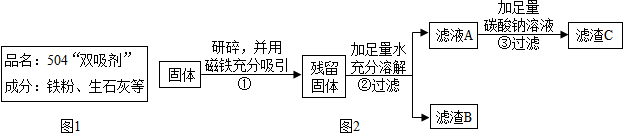
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁与稀盐酸(或稀硫酸)反应生成的氯化铁(或硫酸铁)又与铁粉反应生成氯化亚铁(或硫酸亚铁).
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO(或氧化钙).
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
【反思与评价】甲、乙两同学经过讨论后,完善实验方案最终确定该久置固体的成分是Fe、Fe2O3、CaO、CaCO3.

【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
取少量固体于试管中,滴 加足量的稀盐酸(或稀硫酸). | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe(或铁粉), 一定不含Fe2O3. |
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO(或氧化钙).
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡产生、 澄清石灰水变浑浊、溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
4.日常生活中的下列变化,其中一种与其余三种类别不同的是( )
| A. | 石蜡熔化 | B. | 纸张燃烧 | C. | 粮食霉变 | D. | 烟花爆炸 |
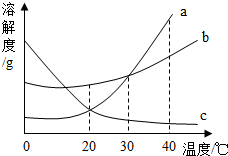 如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: