题目内容
4.某兴趣小组同学为了验证铜、铁、银的金属活动性强弱,进行了如下的实验研究.| 实验设计 | 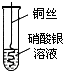 甲 | 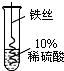 乙 | 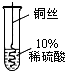 丙 |
| 实验现象 | 观察到现象铜丝上有银白色固体析出 | 铁丝表面有气泡产生 | 铜丝表面无气泡产生 |
| 实验结论 | 金属活动性:铁>铜>银 | ||
②铁丝与稀硫酸反应一段时间后剩余的溶液中,可能含有的溶质是硫酸或H2SO4,为了确定可能含有的溶质,可加入A D(填选项序号)
A.铁 B.氯化钡溶液 C.氯化钠溶液 D.氢氧化铜
③拓展应用:硫酸铜溶液和熟石灰混合,可制农药波尔多液.不能用铁制容器盛放波尔多液的原因是CuSO4+Fe=Cu+FeSO4(用化学方程式表示)
分析 根据取用砂纸打磨过的铜丝插入到盛有硝酸银溶液的试管中,过一会儿取出铜丝,观察到铜丝上有银白色固体析出解答;
①根据配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管、玻璃棒;在量取蒸馏水体积时,若仰视读数,水会量多了,则会导致盐酸的溶质质量分数小于10%解答;
②根据铁和稀硫酸反应的产物是硫酸亚铁和氢气及酸的化学性质解答;
③根据不能用铁制容器盛放波尔多液的原因是:铁与硫酸铜溶液反应生成硫酸亚铁和铜解答.
解答 解:
甲同学设计的实验方案:取用砂纸打磨过的铜丝插入到盛有硝酸银溶液的试管中,过一会儿取出铜丝,观察到铜丝上有银白色固体析出,得出结论铜比银活泼;
①配制10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管、玻璃棒;在量取蒸馏水体积时,若仰视读数,水会量多了,则会导致盐酸的溶质质量分数小于10%;故答案为:玻璃棒;<
②铁和稀硫酸反应的产物是硫酸亚铁和氢气;氢气不容水,最后以气泡从溶液冒出;所以最后剩在溶液中的物质一定有硫酸亚铁,可能含有的溶质是硫酸,为了确定可能含有的溶质,
A、加入铁,如果有气泡生成,则一定有硫酸;
B、加入氯化钡溶液,因为硫酸、硫酸亚铁也能与氯化钡产生沉淀,不能确定一定有硫酸;
C、氯化钠溶液加入后不反应;
D、加入氢氧化铜,硫酸和氢氧化反应生成硫酸铜和水,如果蓝色氢氧化铜溶解,能确定一定有硫酸;
故选AD
③不能用铁制容器盛放波尔多液的原因是:铁与硫酸铜溶液反应生成硫酸亚铁和铜,故答案为:Fe+CuSO4=Cu+FeSO4答案:
答案:铜丝上有银白色固体析出
①玻璃棒<
②硫酸或H2SO4 A、D
③CuSO4+Fe=Cu+FeSO4
点评 金属的活动性顺序是中考的重点内容之一,本题既考查了实验现象的描述、化学方程式的书写,又考查了学生的实验设计能力,综合性比较强,同学们要认真掌握.本考点经常出现在选择题、填空题和实验题中.

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案| A. | MgO+H2SO4→MgSO4+H2O | B. | CuO+CO$\stackrel{高温}{→}$Cu+CO2 | ||
| C. | H2O+CO2→H2CO3 | D. | CaCO3$\stackrel{高温}{→}$CaO+CO2↑ |
| A. | Na2CO3、Ca(OH)2、HCl | B. | KNO3、FeCl3、HCl | ||
| C. | AgNO3、HCl、HNO3 | D. | Ba(NO3)2、Na2CO3、H2SO4 |
| A. | 焚烧秸杆 | B. | 植树造林 | C. | 燃放鞭炮 | D. | 工厂排放烟尘 |
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的CO | 通过足量的氢氧化钠溶液 |
| B | 除去NaOH固体中少量的Na2CO3 | 加足量的稀盐酸 |
| C | 区分NaCl溶液和稀盐酸 | 取样,加入足量NaOH溶液 |
| D | 区分NaOH溶液和Ca(OH)2溶液 | 取样,分别滴加碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | Al能与CuSO4溶液反应,Ag则不能 | |
| B. | Al能与稀盐酸反应,Ag则不能 | |
| C. | 自然界没有以单质形式存在的Al,而有以单质形式存在的Ag | |
| D. | 铝的熔点为660℃,Ag的熔点为962℃ |
 同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液.已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究: