题目内容
如图是甲、乙、丙三种物质的溶解度曲线.根据图中信息回答问题: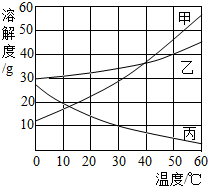
(1)说出甲物质的溶解度随温度变化的规律: .
(2)50℃时,将 40g乙物质加入到80g水中充分溶解后,所得溶液的质量为 .
(3)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数由大到小的顺序是 .

(1)说出甲物质的溶解度随温度变化的规律:
(2)50℃时,将 40g乙物质加入到80g水中充分溶解后,所得溶液的质量为
(3)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数由大到小的顺序是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线可知甲物质的溶解度随温度变化的规律是随着温度的升高,甲物质的溶解度逐渐增大进行解答;
(2)根据50℃时乙物质的溶解度为40g进行解答;
(3)根据甲、乙、丙三物质的溶解度曲线随温度变化的情况分析判断.
(2)根据50℃时乙物质的溶解度为40g进行解答;
(3)根据甲、乙、丙三物质的溶解度曲线随温度变化的情况分析判断.
解答:解:(1)溶解度曲线可知甲物质的溶解度随温度变化的规律是随着温度的升高,甲物质的溶解度逐渐增大;故填:随着温度的升高,甲物质的溶解度逐渐增大;
(2)50℃时乙物质的溶解度为40g,即50℃100g水中最多溶解40g甲物质,所以50℃时,将 40g乙物质加入到80g水中充分溶解后,只能溶解32g甲物质,所得溶液的质量为80g+32g=112g;故填:112g;
(3)丙的溶解度曲线随着温度的降低而升高,所以温度从50℃降低到10℃丙物质没有析出,溶液的质量分数是50℃时饱和溶液的质量分数;甲、乙的溶解度曲线随着温度的降低而降低,所以温度从50℃降低到10℃甲、乙物质析出,从图象可以看出,10℃甲、乙物质的溶解度大小顺序是:乙>甲,都大于50℃时丙物质的溶解度.所以温度降低到10℃时,所得溶液中溶质质量分数由大到小的顺序是乙>甲>丙.故填:乙>甲>丙.
(2)50℃时乙物质的溶解度为40g,即50℃100g水中最多溶解40g甲物质,所以50℃时,将 40g乙物质加入到80g水中充分溶解后,只能溶解32g甲物质,所得溶液的质量为80g+32g=112g;故填:112g;
(3)丙的溶解度曲线随着温度的降低而升高,所以温度从50℃降低到10℃丙物质没有析出,溶液的质量分数是50℃时饱和溶液的质量分数;甲、乙的溶解度曲线随着温度的降低而降低,所以温度从50℃降低到10℃甲、乙物质析出,从图象可以看出,10℃甲、乙物质的溶解度大小顺序是:乙>甲,都大于50℃时丙物质的溶解度.所以温度降低到10℃时,所得溶液中溶质质量分数由大到小的顺序是乙>甲>丙.故填:乙>甲>丙.
点评:本题主要考查了依据物质的溶解度曲线分析问题、解决问题的能力,能较好的考查出学生对知识的掌握和应用情况.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
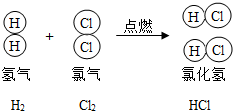 归纳与反思是学习过程中的重要环节之一.如图所示是教科书的一幅插图,“点燃”两字是某同学做的听课笔记.下列几位同学复习时对图中蕴含知识的归纳错误的是( )
归纳与反思是学习过程中的重要环节之一.如图所示是教科书的一幅插图,“点燃”两字是某同学做的听课笔记.下列几位同学复习时对图中蕴含知识的归纳错误的是( )| A、该反应的生成物易溶于水,所得溶液的pH<7 | ||||
B、此反应为H2+Cl2
| ||||
| C、反应物和生成物之间的质量比为1:1:2 | ||||
| D、该反应说明燃烧不一定要有O2,但必须有助燃物质,如Cl2 |
下列说法中正确的是( )
| A、酸的溶液显酸性,所以显酸性的溶液一定是酸的溶液 |
| B、离子是带电的原子或原子团,所以带电的微粒一定是离子 |
| C、碱的溶液显碱性,但显碱性溶液不一定是碱溶液 |
| D、向某物质中加入稀盐酸产生无色无味气体,则该物质中一定含有碳酸根离子或碳酸氢根离子 |
 如图是甲、乙、丙三种固体的溶解度曲线.
如图是甲、乙、丙三种固体的溶解度曲线. 如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.
如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.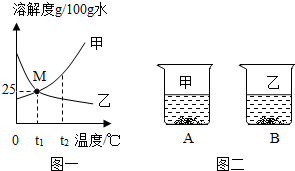 图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.
图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.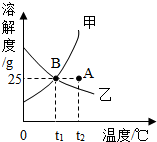 如图为甲、乙两种固体物质在水中的溶解度曲线:
如图为甲、乙两种固体物质在水中的溶解度曲线: