题目内容
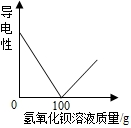
向100克硫酸溶液滴加17.1%的氢氧化钡溶液,一边滴加,一边测定溶液的导电性,溶液的导电性随氢氧化钡溶液质量增加而变化,如图所示. 求稀硫酸溶液中溶质的质量分数.
【答案】分析:据图可看出当氢氧化钡溶液的质量加到100克时,溶液不导电,此时硫酸与氢氧化钡恰好完全反应.利用硫酸与氢氧化钡反应的化学方程式,根据氢氧化钡的质量求出硫酸的质量,再用 ×100%即可求出稀硫酸溶液中溶质的质量分数.
×100%即可求出稀硫酸溶液中溶质的质量分数.
解答:解:设硫酸的质量为x
H2SO4+Ba(OH)2=2H2O+BaSO4↓
98 171
x 100g×17.1%=17.1g
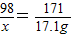
x=9.8g
稀硫酸溶液中溶质的质量分数=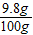 ×100%=9.8%
×100%=9.8%
答:稀硫酸溶液中溶质的质量分数是9.8%.
点评:本题并不难,是一道基本的根据化学方程式计算题,解题关键是要会看图,会根据图中的溶液导电性情况确定什么时候硫酸与氢氧化钡恰好完全反应.
 ×100%即可求出稀硫酸溶液中溶质的质量分数.
×100%即可求出稀硫酸溶液中溶质的质量分数.解答:解:设硫酸的质量为x
H2SO4+Ba(OH)2=2H2O+BaSO4↓
98 171
x 100g×17.1%=17.1g
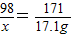
x=9.8g
稀硫酸溶液中溶质的质量分数=
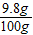 ×100%=9.8%
×100%=9.8%答:稀硫酸溶液中溶质的质量分数是9.8%.
点评:本题并不难,是一道基本的根据化学方程式计算题,解题关键是要会看图,会根据图中的溶液导电性情况确定什么时候硫酸与氢氧化钡恰好完全反应.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
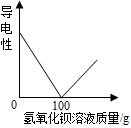 向100克硫酸溶液滴加17.1%的氢氧化钡溶液,一边滴加,一边测定溶液的导电性,溶液的导电性随氢氧化钡溶液质量增加而变化,如图所示. 求稀硫酸溶液中溶质的质量分数.
向100克硫酸溶液滴加17.1%的氢氧化钡溶液,一边滴加,一边测定溶液的导电性,溶液的导电性随氢氧化钡溶液质量增加而变化,如图所示. 求稀硫酸溶液中溶质的质量分数.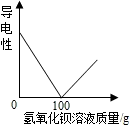 向100克硫酸溶液滴加17.1%的氢氧化钡溶液,一边滴加,一边测定溶液的导电性,溶液的导电性随氢氧化钡溶液质量增加而变化,如图所示. 求稀硫酸溶液中溶质的质量分数.
向100克硫酸溶液滴加17.1%的氢氧化钡溶液,一边滴加,一边测定溶液的导电性,溶液的导电性随氢氧化钡溶液质量增加而变化,如图所示. 求稀硫酸溶液中溶质的质量分数.