题目内容
16.在测定空气中氧气含量的实验时,甲同学的集气瓶内水面上升明显小于瓶内空气的$\frac{1}{5}$,乙同学的结果明显大于$\frac{1}{5}$.下列对这两种现象原因分析合理的是( )| A. | 甲同学插入燃烧匙太慢 | B. | 甲同学的装置漏气 | ||
| C. | 乙同学可能使用红磷不足 | D. | 乙同学没冷却到室温就打开弹簧夹 |
分析 如果装置漏气,或红磷不足,或没有冷却至室温就打开弹簧夹,都能够导致进入集气瓶中的水不到集气瓶容积的五分之一;
如果插入燃烧匙太慢,或没有夹紧止水夹,都能够导致进入集气瓶中的水多于集气瓶容积的五分之一.
解答 解:A、插入燃烧匙太慢时,会导致集气瓶中的气体受热膨胀外逸,从而导致进入集气瓶中的水多于集气瓶容积的五分之一,即导致结果明显大于五分之一,该选项分析不合理;
B、装置漏气时,会导致进入集气瓶中的水不到集气瓶容积的五分之一,从而导致集气瓶内水面上升明显小于瓶内空气的五分之一,该选项分析合理;
C、使用红磷不足时,会导致进入集气瓶中的水不到集气瓶容积的五分之一,从而导致集气瓶内水面上升明显小于瓶内空气的五分之一,该选项分析合理;
D、没冷却到室温就打开弹簧夹,会导致进入集气瓶中的水不到集气瓶容积的五分之一,从而导致集气瓶内水面上升明显小于瓶内空气的五分之一,该选项分析合理.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
7.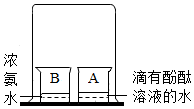 学习小组的同学在探究分子的性质,请你参与并完成相关的问题.
学习小组的同学在探究分子的性质,请你参与并完成相关的问题.
【进行实验】(如图)观察到的现象是A中溶液逐渐变为红色,结论为分子是不断运动的.
【交流与讨论】有同学对A中溶液的变红提出了以下猜想:提出了猜想1:A中溶液变红也可能是A中溶液放置一段时间后,自动就会变红;
猜想2:大烧杯内壁附着的某种物质挥发出来使A中溶液变红.
【再次实验】请你选择其中一个猜想并设计实验进行验证.
 学习小组的同学在探究分子的性质,请你参与并完成相关的问题.
学习小组的同学在探究分子的性质,请你参与并完成相关的问题.【进行实验】(如图)观察到的现象是A中溶液逐渐变为红色,结论为分子是不断运动的.
【交流与讨论】有同学对A中溶液的变红提出了以下猜想:提出了猜想1:A中溶液变红也可能是A中溶液放置一段时间后,自动就会变红;
猜想2:大烧杯内壁附着的某种物质挥发出来使A中溶液变红.
【再次实验】请你选择其中一个猜想并设计实验进行验证.
| 实验操作 | 实验现象 | 实验结论 |
| 取一烧杯,加入适量的水,再滴入几滴酚酞试液,置于桌面上静置一段时间 | 溶液不变色 | 猜想一正确 |
11.苯甲酸(C6H5COOH)是一种有机酸,可用作食品防腐剂,其酸性比碳酸强.下列有关推测不合理的是( )
| A. | 苯甲酸溶于水能解离出大量OH- | |
| B. | 苯甲酸溶于水能解离出大量H+ | |
| C. | 苯甲酸溶液能使紫色石蕊试液变红色 | |
| D. | 苯甲酸溶液不能使无色酚酞试液变色 |
1.对下列化学用语中数字“2”的说法正确的是( )
①2N、②2CO、③SO2、④$\stackrel{+2}{Ca}$O、⑤Mg2+、⑥2OH-、⑦H2O.
①2N、②2CO、③SO2、④$\stackrel{+2}{Ca}$O、⑤Mg2+、⑥2OH-、⑦H2O.
| A. | 表示离子所带电荷数的是④⑤ | B. | 表示分子个数的是①② | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示离子个数的是⑤⑥ |
5.已知镁可以在氮气中燃烧生成氮化镁,若在氮化镁中氮元素的化合价为-3价,则氮化镁的化学式为( )
| A. | MgN | B. | Mg2N3 | C. | Mg3N2 | D. | MgN2 |
6.下列化学反应方程式书写正确的是( )
| A. | 木炭在空气中燃烧:C+O2═CO2↑ | |
| B. | 镁在空气中燃烧:Mg+O2═MgO2 | |
| C. | 实验室制取二氧化碳:CaCO3+2HCl═CaCl2+CO2↑+H2O | |
| D. | 在双氧水中加入二氧化锰:H2O2═H2O+O2↑ |