题目内容
实验室有一瓶硫酸废液,老师请小红同学设计方案测定该废液中硫酸的质量分数。小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入适量的硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去掉铁锈)放入该小烧杯中反应,当反应后的溶液呈中性时再次称量,总质量为43.9 g。请回答下列问题:
反应中产生的气体的质量是。
计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。
如果铁钉的铁锈未除净,对计算结果的影响是 (选填“偏大”、“偏小”、“无影响”) 。
(1)0.1g ………………………… (1分)
(2) 解:设参加反应硫酸的质量为x
Fe+H2SO4== FeSO4+ H2↑
98 2
X 0.1g
98 :X = 2:0.1g
X =4.9g
硫酸的质量分数为(4.9/33.2-18.2)×100%=32.7%……… (1分)
(3)偏小 ………………………… (1分)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
金刚石、石墨和C60都是由碳元素组成的单质,下列说法正确的是( )
| A.碳原子的排列方式相同 |
| B.在氧气中充分燃烧时都生成二氧化碳 |
| C.物理性质相同 |
| D.一定条件下,石墨转化成金刚石是物理变化 |
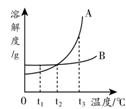 右图是A、B两种固
右图是A、B两种固 体物质的溶解度曲线,下列说法正确的是
体物质的溶解度曲线,下列说法正确的是
 应,生成NaHCO3,写出此反应的化学方程式为___________________。
应,生成NaHCO3,写出此反应的化学方程式为___________________。
 木条伸入集气瓶中 D.向集气瓶中加入澄清石灰水,振荡
木条伸入集气瓶中 D.向集气瓶中加入澄清石灰水,振荡 是21世纪的重要金属材料,它在元素周期表中的某些信息如下图所示。下列有关钛的说法正确的是
是21世纪的重要金属材料,它在元素周期表中的某些信息如下图所示。下列有关钛的说法正确的是 .87g
.87g 