题目内容
1909年,化学家哈伯用氮气和氢气在高温高压条件下首次合成了氨气,反应原理是N2+3H2 2NH3。氨气具有可燃性,燃烧时发热量高。近年科学家发现用催化剂在常温下就能合成氨气,使其有望成为替代氢能的新一代能源。
2NH3。氨气具有可燃性,燃烧时发热量高。近年科学家发现用催化剂在常温下就能合成氨气,使其有望成为替代氢能的新一代能源。
(1)氨气中氮元素的化合价是___;氨气中氮元素与氢元素的质量比为____。
(2)若用下面三幅模型图表示合成氨气的过程,则从反应开始到完成的排列顺序是_____(用字母表示)。
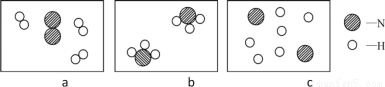
(3)氨气燃烧时可能会生成氮氧化物而污染环境,但在一定条件下,氨气燃烧却没有任何污染,该反应原理是:4NH3+3O2 2X+6H2O,其中X是________。
2X+6H2O,其中X是________。
练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
除去下列物质中含有的少量杂质,所选用的试剂不合理的是( )
序号 | 混合物 | 除杂试剂 |
A | 一氧化碳中混有少量二氧化碳 | 足量的氢氧化钠溶液 |
B | 铁粉中混有少量氧化铜 | 足量的稀硫酸 |
C | 氯化亚铁溶液混有少量氯化铜 | 足量的铁粉 |
D | 氯化钙溶液中混有少量盐酸 | 过量的碳酸钙 |
A. A B. B C. C D. D



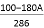 g D. (100-A?a%)g
g D. (100-A?a%)g