题目内容
9.某品牌纯碱中含有杂质NaCl,化学兴趣小组同学进行探究:称取10g样品放入烧杯中,加入稀盐酸92.2g恰好反应完全.称得反应后物质的总质量为100g,请你计算:(1)反应产生气体的质量为2.2g.
(2)计算样品中纯碱的质量分数(写出详细过程).
分析 根据质量守恒定律,化学反应前后物质的总质量不变,向碳酸钠和氯化钠的固体混合物中加入稀盐酸,只是碳酸钠与盐酸反应,反应后生成了二氧化碳气体不存在于溶液中,可以求得二氧化碳的质量;依据二氧化碳的质量利用方程式可以求出碳酸钠的质量,进而可求碳酸钠的质量分数.
解答 解:(1)由质量守恒定律可知,生成的二氧化碳的质量=10g+92.2g-100g=2.2g;
(2)设原固体混合物中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{44}=\frac{x}{2.2g}$ 解得:x=5.3g
样品中纯碱的质量分数:$\frac{5.3g}{10g}×$100%=53%
故答为:(1)2.2;(2)计算样品中纯碱的质量分数是53%.
点评 本题通过计算的形式考查了碳酸盐与酸的反应,解答本题的关键是根据质量守恒定律来进行计算是要计算生成的二氧化碳的质量.

练习册系列答案
相关题目
19.下列反应不属于置换反应的是( )
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | Fe+CuSO4═FeSO4+Cu |
4.把17.1g氯化钠和碳酸钠的混合物,加入100g7.3%的盐酸中,恰好完全反应.计算:
(1)生成气体的质量和体积(标准状况下二氧化碳的密度为1.96g/L).
(2)反应后所得溶液中溶质的质量分数.
(1)生成气体的质量和体积(标准状况下二氧化碳的密度为1.96g/L).
(2)反应后所得溶液中溶质的质量分数.
1.一块4克的合金,与足量的盐酸反应,产生0.2克氢气,则该合金的组成可能为( )
| A. | Fe Mg | B. | Fe Al | C. | Fe Zn | D. | Al Mg |
18.下列物质能通过金属与酸反应制得的是 ( )
| A. | CuCl2 | B. | MgSO4 | C. | Fe2(SO4)3 | D. | FeCl2 |
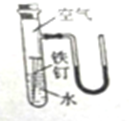 如图是某研究的实验装置,几天以后:
如图是某研究的实验装置,几天以后: