题目内容
科学家经过研究,发现二氧化碳也是一种宝贵的碳氧资源.以CO2和NH3为原料合成尿素[CO(NH2)2]是同定和利用CO2的成功范例.它还可以与氢气反应生成多种有 机物,如甲烷(CH4)、乙烯(C2H4)等.试计算:
(1)CH4中碳、氢元素的质量比 .
(2) CO(NH2)2中氮元素的质量分数 .(计算结果精确到0.1%)
(3) CO2转化为C2H4的化学方程式为:2CO2+6H2一定条件C2H4+4H2O,若用24g H2转化CO2,则理论上能生成C2H4多少克(列式计算)?
解:(1)相对原子质量与原子个数乘积的比是元素的质量比.
则有12:4=3:1
故答案为:3:1
(2)某元素的质量分数= ×100%
则有尿素中氮元素的质量分数是: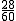 ×100%≈46.7%;
×100%≈46.7%;
故答案为:46.7%
(3)设理论上能生成C2H4的质量是x
2CO2+6H2一定条件C2H4+4H2O
12 28
24g x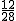 =
= 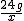
x=56g
答:理论上可生成C2H4的质量是56g
解析

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目