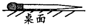题目内容
2.关注健康,预防疾病.下列叙述正确的是( )| A. | 人体胃液正常的pH范围在0.5-1.9 | |
| B. | 人体缺乏维生素A会引起坏血病 | |
| C. | 铁、碘、氟、钠、硒是人体所需的微量元素 | |
| D. | 人体缺碘会引起甲状腺肿大,碘过量也会引起甲状腺肿大 |
分析 A、根据人体胃液正常的pH范围进行分析判断.
B、根据维生素的生理作用进行分析判断.
C、根据人体所需的微量元素进行解答;
D、根据碘的生理功能和缺乏症进行分析判断.
解答 解:A、人体胃液正常的pH范围在0.9-1.5 之间,故选项说法错误.
B、人体缺乏维生素A会引起夜盲症,不是坏血病,故选项说法错误.
C、钠是常量元素,不是微量元素,故选项说法错误.
D、碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大;碘过量也会引起甲状腺肿大,故选项说法正确.
答案:D
点评 与人类生产生活相关的化学知识是中考的热点,了解生活中常见的有毒物质(甲醛、亚硝酸钠等)、微量元素、六大营养素的相关知识的相关知识即可正确解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9. 图A为镁原子的结构示意图,图B为镁元素在元素周期表中的部分信息.下列叙述错误的是( )
图A为镁原子的结构示意图,图B为镁元素在元素周期表中的部分信息.下列叙述错误的是( )
 图A为镁原子的结构示意图,图B为镁元素在元素周期表中的部分信息.下列叙述错误的是( )
图A为镁原子的结构示意图,图B为镁元素在元素周期表中的部分信息.下列叙述错误的是( )| A. | 镁离子核外有两个电子层 | |
| B. | 镁原子在化学反应中易失去电子 | |
| C. | 镁元素的原子序数等于镁元素原子的核内质子数 | |
| D. | 由于元素原子的核外电子层数与元素所在的周期数相同,可知镁元素位于第2周期 |
17.有关物质的检验、鉴别、除杂,下列说法正确的是( )
| A. | 把燃着的木条伸入某集气瓶内,木条熄灭,说明瓶内的气体是CO2 | |
| B. | 用点燃的方法除去CO2中少量的CO | |
| C. | 不用另加试剂就可以把MgSO4、KOH、HCl、BaCl2四种溶液鉴别出来 | |
| D. | 向某溶液中加入BaCl2溶液,产生白色沉淀,过滤后往沉淀中加入足量的稀硝酸,沉淀部分溶解并产生气泡,说明溶液中可能含有硫酸根离子 |
11.食用下列食品,通常不会对人体健康造成危害的是( )
| A. | 用甲醛溶液浸泡海鲜品 | B. | 用工业酒精勾兑引用酒 | ||
| C. | 牛奶经发酵后得到酸奶 | D. | 霉变变质的大米、花生 |

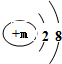 其微粒符号可表示为A2-,则m的值8
其微粒符号可表示为A2-,则m的值8