题目内容
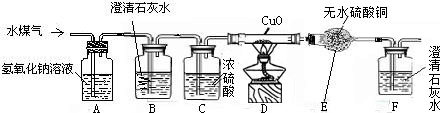
工业上用赤热的焦炭和水蒸气在高温条件下生产水煤气,其产物中含有H2O、H2、CO、CO2等物质.课外兴趣小组的同学设计如下实验装置,用来证明水煤气中含有H2和CO,请根据下图回答有关问题:(装置图中省去了铁架台)
(1)装置B、C的作用分别是
(2)证明水煤气中有H2的现象是
(3)小华同学认为该装置还可用来测定氧化铜中铜、氧元素质量比.他记录了以下两个数据:反应前D装置中氧化铜样品为Xg,反应后F装置增重Yg,则氧化铜中铜、氧元素质量比的计算式为
(4)该装置的设计,有一处明显的不足,应如何改进
分析:要证明一氧化碳和氢气的存在,可以从这两种物质反应后生成的二氧化碳和水进行证明,二氧化碳能使澄清石灰水变浑浊,水能使无水硫酸铜变蓝,一氧化碳是有毒的气体,使用后必须进行尾气处理.
解答:解:(1)水煤气中含有二氧化碳和水,使用澄清石灰水的目的是检验其中的二氧化碳是否被除尽,浓硫酸具有吸水性,能将水煤气中的水分除去,所以本题答案为:检验二氧化碳是否除尽,除水;
(2)氢气具有还原性,能将氧化铜还原为红色的铜,生成的水能使无水硫酸铜变蓝,所以本题答案为:氧化铜粉末逐渐变红,且无水硫酸铜变蓝;
(3)反应后F装置增重Yg,说明生成的二氧化碳的质量为Yg,设生成的铜的质量为x
CuO+CO
Cu+CO2
64 44
X Yg
=
x=
所以氧元素的质量为:Xg-
,所以铜氧两种元素的质量比为:16Y:(11X-16Y)
氢氧化钙吸收二氧化碳不完全,则会导致二氧化碳的质量偏大,求得的铜元素的质量偏大而氧元素质量偏小,会导致比值偏大,所以本题答案为:16Y:(11X-16Y),偏大.
(4)一氧化碳是有毒的气体,必须进行尾气处理,以防造成空气污染,所以本题答案为:没有进行尾气处理,可收集或直接点燃.
(2)氢气具有还原性,能将氧化铜还原为红色的铜,生成的水能使无水硫酸铜变蓝,所以本题答案为:氧化铜粉末逐渐变红,且无水硫酸铜变蓝;
(3)反应后F装置增重Yg,说明生成的二氧化碳的质量为Yg,设生成的铜的质量为x
CuO+CO
| ||
64 44
X Yg
| 64 |
| x |
| 44 |
| Yg |
x=
| 16Yg |
| 11 |
所以氧元素的质量为:Xg-
| 16Yg |
| 11 |
氢氧化钙吸收二氧化碳不完全,则会导致二氧化碳的质量偏大,求得的铜元素的质量偏大而氧元素质量偏小,会导致比值偏大,所以本题答案为:16Y:(11X-16Y),偏大.
(4)一氧化碳是有毒的气体,必须进行尾气处理,以防造成空气污染,所以本题答案为:没有进行尾气处理,可收集或直接点燃.
点评:本题考查了一氧化碳和氢气存在的检验,完成此题,可以依据已有的知识进行,检验氢气的存在是根据反应后生成的水进行,检验一氧化碳的存在是根据反应后生成的二氧化碳进行.

练习册系列答案
相关题目

 Cu+H2O CO+CuO
Cu+H2O CO+CuO
