题目内容
7.现有下列仪器,回答有关问题: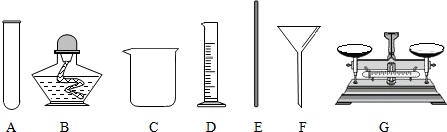
(1)仪器C的用途是配制溶液和较大量试剂的反应容器.
(2)要配制一定溶质质量分数的硝酸钾溶液.
①从上图选择所需仪器,除E、G外,还需选用的仪器有CD(填字母);
②配制的步骤为计算、称量、量取、溶解、装入试剂瓶并贴好标签;
③此实验中E的作用是搅拌,加快溶解速率.
分析 (1)根据烧杯可以用来作为配制溶液和较大量试剂的反应容器进行分析;
(2)根据配制一定溶质质量分数溶液需要的仪器,配制步骤等进行分析.
解答 解:(1)仪器C是烧杯,烧杯可以用来作为配制溶液和较大量试剂的反应容器;
(2)①从上图选择所需仪器,除玻璃棒、天平外,还需选用的仪器有烧杯、量筒,故选:CD;
②配制的步骤为计算、称量、量取、溶解、装入试剂瓶并贴好标签;
③实验中玻璃棒的作用是:搅拌,加快溶解速率.
故答案为:(1)配制溶液和较大量试剂的反应容器;
(2)①CD;
②称量;
③搅拌,加快溶解速率.
点评 本题主要考查常用仪器的作用和认识,难度不大,需要理解、识记.

练习册系列答案
相关题目
17.同学们围绕“铁在氧气里燃烧”的实验展开以下探究活动.
活动一:探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系
【实验探究】
【拓展延伸】
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验,若用排水法收集一瓶体积分数为90%的氧气,预先应向容积为400mL的集气瓶中加水,水的体积约为350mL.
活动二:探究铁燃烧时溅落下来的黑色物质中是否有铁单质
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
②铁的氧化物均能溶于酸.
【实验探究】
【拓展延伸】
已知:高温条件下铁和水能反应生成四氧化三铁和氢气,则该反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.由此可知探究活动二中为了防止集气瓶炸裂,应采取的措施是在集气瓶底部铺一层细沙.
活动一:探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系
【实验探究】
| 实验操作 | 实验现象 | 解释与结论 |
| 实验1:取直径0.20mm,含碳0.1%的铁丝,在氧气中燃烧 | 零星的火星 | ①铁燃烧的化学方程式是3Fe+2O2$\frac{\underline{\;高温\;}}{\;}$Fe3O4 ②铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为含碳量越高,火星越明显 |
| 实验2:取直径0.20mm ,含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 |
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验,若用排水法收集一瓶体积分数为90%的氧气,预先应向容积为400mL的集气瓶中加水,水的体积约为350mL.
活动二:探究铁燃烧时溅落下来的黑色物质中是否有铁单质
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
②铁的氧化物均能溶于酸.
【实验探究】
| 实验操作 | 实验现象 | 解释与结论 |
| 将冷却后的黑色固体碾碎,装入试管,加入稀盐酸 | 有气泡产生 | 铁燃烧时溅落下来的黑色固体中含有铁单质 |
已知:高温条件下铁和水能反应生成四氧化三铁和氢气,则该反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.由此可知探究活动二中为了防止集气瓶炸裂,应采取的措施是在集气瓶底部铺一层细沙.
15.下列实验现象描述不正确的是( )
| A. | 木炭在氧气中燃烧发出白光,放出热量 | |
| B. | 向氢氧化钠溶液中加入硫酸铜溶液有蓝色沉淀生成 | |
| C. | 纯净的氢气在空气中燃烧产生淡蓝色火焰 | |
| D. | 向盛有铁锈的试管中加入稀盐酸,反应后得到浅绿色的溶液 |
12.下列物质变化属于化学变化的是( )
| A. | 铁生锈 | B. | 汽油挥发 | C. | 石蜡熔化 | D. | 滴水成冰 |
19.制造下列物品所使用的材料,不属于有机合成材料的是( )
| A. |  塑料保鲜盒 | B. |  真丝围巾 | C. |  涤纶服装 | D. |  汽车轮胎 |
 某小组在科学社团课上了解到氨水是由氨气溶于水并与水发生反应形成的.氨水中除NH3、H2O外,还有氨气和水发生反应的生成物,其中的生成物使氨水呈碱性.小组同学想用所学的知识对“氨气和水反应的生成物使氨水呈碱性”进行验证.
某小组在科学社团课上了解到氨水是由氨气溶于水并与水发生反应形成的.氨水中除NH3、H2O外,还有氨气和水发生反应的生成物,其中的生成物使氨水呈碱性.小组同学想用所学的知识对“氨气和水反应的生成物使氨水呈碱性”进行验证.