题目内容
人体缺少必需的微量元素会影响健康,患佝偻病通常需要补充的元素是( )
| A. | 铁 | B. | 钙 | C. | 氟 | D. | 碘 |
B

已知,相同温度下,在溶液中进行的化学实反应的快慢(化学反应速率)既与单位体积内参加反应的溶质质量(微粒数目)有关,也与参加反应的固体跟溶液的接触面积有关.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的化学方程式有① ;②
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验,将表中所给的混合溶液(混合前后溶液的体积变化忽略不计)分别加入到6个盛有过量等量锌粒(锌粒与溶液的接触面积相同)的反应瓶中,收集产生的气体,记录获得同样多的气体所需的时间.21世纪教育网
实验混合溶液 | A | B | C | D | E | F |
28%稀硫酸/m/L | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液m/L | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 8 | 0 |
①请完成此实验设计,其中:V1= ;V6= ;V9= ;
②反应一段时间后,实验A中的金属呈 色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因
由以下粒子结构示意图得出的结论中错误的是( )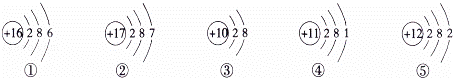
|
| A. | 在化合物中,①可显﹣2价,⑤可显+2价 |
|
| B. | ①②为非金属元素的原子,④⑤为金属元素的原子 |
|
| C. | ③为相对稳定结构,一般不容易参加化学反应 |
|
| D. | 上述粒子在发生化学反应时,其质子数、电子数均发生改变 |
化学物质及其变化同日常生活密切相关。
(1)检验市场上销售的食盐中是否有碘元素(元素符号为I)的一种方法,
是在酸性条件下,使食盐样品溶液跟一种试剂X反应
(KIO3+5X+6HCl==6KCl+3I2+3H2O),如果样品中含有碘元素,则会生成
能够使淀粉试纸变蓝的碘单质。这种试剂X是__ 。
(2)按下表中浸液配方可制无泥皮蛋。配制浸液时,是否可以用生石灰和
纯碱(Na2CO3)代替氢氧化钠和氢氧化钙?请用化学方程式说明理由。
| 浸液配方(可浸泡4只鸭蛋) NaOH 6g NaCl 10g Ca(OH)2 59g 茶叶 5g H2O 210mL |
(3)调味用的食醋中含有醋酸(用HAc表示其组成),可用来浸泡除去壶
中的水垢(主要成分是碳酸钙和氢氧化镁)。写出有关反应的化学方程式。

 B2的相对分子质量。
B2的相对分子质量。 请回答:
请回答: C.甲状腺肿大
C.甲状腺肿大