题目内容
8.在Cu(NO3)2、AgNO3的混合液中加入一定量的铁粉,充分反应后过滤,在滤液中滴加稀盐酸,有白色沉淀生成,则滤渣中一定含有的固体是银,写出生成白色沉淀的方程式HCl+AgNO3═AgCl↓+HNO3.分析 金属与盐发生置换反应生成金属和盐,把铁粉加到AgNO3和Cu(NO3)2的混合溶液中,充分反应后过滤,所得滤渣一定为金属单质,且是铁、铜、银中的一种或几种.往得到的滤液中滴稀盐酸,有白色沉淀生成,则滤液中一定有剩余的硝酸银,故硝酸铜未参与反应,得到的金属一定是银.
解答 解:根据金属与盐发生置换反应生成金属和盐,则Fe与AgNO3反应生成Fe(NO3)2和银、与Cu(NO3)2反应生成Fe(NO3)2和铜,根据金属活动性,铁粉会先和硝酸银反应,然后和硝酸铜反应,往得到的滤液中滴稀盐酸,有白色沉淀生成,则滤液中一定有剩余的硝酸银,硝酸铜未参与反应,铁不足,滤渣中含有银,化学方程式是HCl+AgNO3═AgCl↓+HNO3.
故答案为:银,HCl+AgNO3═AgCl↓+HNO3
点评 题中的“往滤液中加入稀盐酸,白色沉淀产生”是个重要现象,这个现象隐藏了“硝酸银过量”的关键性条件,本题考查了金属活动性顺序的应用.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
18.下列图示实验操作中,正确的是( )
| A. |  | B. | 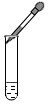 | C. |  | D. |  |
19.构成物质的微粒有多种,下列物质由分子构成的是( )
| A. | 氯化钠 | B. | 水 | C. | 硫 | D. | 水银(Hg) |
13.下列关于物质燃烧的现象描述正确的是( )
| A. | 木炭燃烧后生成二氧化碳 | |
| B. | 铁丝伸入盛有氧气的集气瓶中剧烈燃烧、火星四射 | |
| C. | 红磷在空气中燃烧产生大量白雾 | |
| D. | 硫在空气中燃烧发出淡蓝色火焰 |
17.写出下列符号或符号的意义
| 符号 | 意义 | 符号 | 意义 |
| H | 氢元素 | Fe | 铁元素 |
| 一个氢原子 | 一个铁原子 | ||
| H+ | 一个氢离子 | 铁这种物质 | |
| Na+ | 一个钠离子 | 2O | 2个氧原子 |
| 5Cl- | 5个氯离子 | 3H2 | 3个氢分子 |
 表示氧原子,用
表示氧原子,用 表示氢原子,请按要求回答下列问题.
表示氢原子,请按要求回答下列问题.