题目内容
20.氧的原子核带8个单位正电荷,核外有8个电子.相对原子质量=质子数+中子数,氧的相对原子质量为16,则这种氧的原子核中有8个中子.分析 根据相对原子质量=质子数+中子数,在原子中,核内质子数=核外电子数=核电荷数,进行分析解答本题.
解答 解:在原子中,核内质子数=核外电子数=核电荷数,氧的原子核带8个单位正电荷,核外有8个电子,质子数为8;相对原子质量=质子数+中子数,氧的相对原子质量为16,则这种氧的原子核中含中子数为16-8=8.
故答案为:8;8.
点评 本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数.

练习册系列答案
相关题目
13.在下列各组中,若两种氧化物组成的固体混合物5.6克恰好与100克7.3%的盐酸完全反应,则该混合物可能是( )
| A. | MgO和ZnO | B. | CaO和MgO | C. | CaO和CuO | D. | CuO和ZnO |
8.碳酸氢铵(NH4HCO3)受热分解生成的混合气体(在100℃以上),该气体的平均摩尔质量为( )
| A. | 52.7g/mol | B. | 31g/mol | C. | 26.3g/mol | D. | 23.6g/mol |
5.下列有关构成物质粒子的说法,正确的是( )
| A. | 分子一定比原子大 | |
| B. | 分子、原子都是化学变化中的最小粒子 | |
| C. | 物质状态发生变化,是因为粒子大小发生变化 | |
| D. | 分子、原子都是构成物质的粒子 |
12.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.下列操作顺序中最合适的是( )
| A. | ②④⑤①③ | B. | ⑤④②③① | C. | ②⑤④①③ | D. | ⑤②④③① |

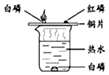 如图所示的一组实验可用于研究燃烧的条件.已知白磷的着火点是40℃,红磷的着火点是240℃.
如图所示的一组实验可用于研究燃烧的条件.已知白磷的着火点是40℃,红磷的着火点是240℃.