题目内容
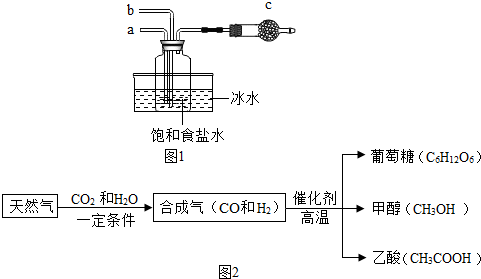
3.天然气的主要成分是甲烷,现将3.2g甲烷在氧气中完全燃烧,生成二氧化碳8.8g,水7.2g,则甲烷的组成中( )| A. | 只含有碳、氢元素 | |
| B. | 一定含有碳、氢、氧元素 | |
| C. | 一定含有碳、氢元素,可能含有氧元素 | |
| D. | 一定含有碳、氧元素,可能含有氢元素 |
分析 根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素.
解答 解:8.8gCO2中含有碳元素的质量为:8.8g×$\frac{12}{44}×$100%=2.4g,7.2g水中含有氢元素的质量为:7.2g×$\frac{1×2}{18}$×100%=0.8g,生成物8.8g二氧化碳和7.2g水中所含碳、氢元素的质量和=2.4g+0.8g=3.2g,3.2g=3.2g,则该物质中一定含有碳、氢两种元素,一定不含氧元素.
A、由上述分析可知,该物质中一定含有碳、氢两种元素,一定不含氧元素,故选项说法正确.
B、由上述分析可知,该物质中一定含有碳、氢两种元素,一定不含氧元素,故选项说法错误.
C、由上述分析可知,该物质中一定含有碳、氢两种元素,一定不含氧元素,故选项说法错误.
D、由上述分析可知,该物质中一定含有碳、氢两种元素,一定不含氧元素,故选项说法错误.
故选:A.
点评 本题难度稍大,主要考查了质量守恒定律、化学式的计算,解题的关键是根据质量守恒定律确定确定物质的元素组成.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
13.黑木耳、大枣中富含铁,这里“铁”是指( )
| A. | 单质 | B. | 元素 | C. | 原子 | D. | 分子 |
14.“墙角数枝梅,凌寒独自开;遥知不是雪,为有暗香来.”“为有暗香来”说明( )
| A. | 分子在不断运动 | B. | 分子的质量很小 | C. | 分子之间有间隔 | D. | 分子的体积很小 |
8.蜡烛的主要成分是石蜡,刚熄灭时,烛芯会冒出一缕白烟,燃着的火柴只要碰到白烟,便能使蜡烛复燃.此白烟可能是( )
| A. | 石蜡气体 | B. | 水蒸气 | ||
| C. | 二氧化碳气体 | D. | 石蜡的固体小颗粒 |
3.下列是生活中常见的一些变化,其中属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 海水晒盐 | C. | 潮涨潮落 | D. | 干冰升华 |
1.下列对实验现象的观察或记录中正确的是( )
| A. | 将黄铜与铜互相刻划,铜表面出现划痕 | |
| B. | 镁在空气中燃烧,发出白光,生成氧化镁固体 | |
| C. | 室温下,向饱和食盐水中加入少量硝酸钾固体、搅拌,固体不溶解 | |
| D. | 向蒸馏水中滴入2-3滴植物油,搅拌,植物油完全溶解 | |
| E. | 将黄铜与铜互相刻划,铜表面出现划痕 |