题目内容
实验室通常用电石(主要成分为CaC2)和水反应制取乙炔(C2H2),反应的方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑.若用含CaC2质量为128g的电石和水反应,理论上可收集到乙炔的质量是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据碳化钙的质量,通过化学方程式中的质量比可以计算制取的碳化钙的质量.
解答:解:设:收集到乙炔的质量为x
CaC2+2H2O═Ca(OH)2+C2H2↑
64 26
128 g x
=
x=52g
答:理论上收集到乙炔52 g.
CaC2+2H2O═Ca(OH)2+C2H2↑
64 26
128 g x
| 64 |
| 128g |
| 26 |
| x |
x=52g
答:理论上收集到乙炔52 g.
点评:本题比较简单,主要考查运用化学方程式进行计算的能力;要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识是解答关键.

练习册系列答案
相关题目
下列变化中属于物理变化的是( )
| A、牛奶变酸 | B、铁锅生锈 |
| C、米饭变馊 | D、玻璃杯破碎 |
下列各种食物中蛋白质含量最丰富的是( )
A、 草莓 |
B、 西红柿 |
C、 馒头 |
D、 鸡蛋 |
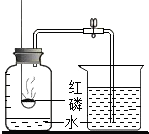 测定空气中氧气含量的实验装置如图所示,实验步骤如下:
测定空气中氧气含量的实验装置如图所示,实验步骤如下:
