题目内容
15.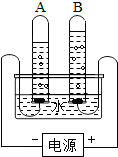 如图是实验室电解水的简易装置示意图.
如图是实验室电解水的简易装置示意图.(1)接通直流电源后A试管产生的是氢气,B试管产生的是氧气.
(2)检验B试管内气体的方法是用带火星的木条检验,观察木条是否复燃.
(3)反应一段时间后,A试管与B试管内气体的体积比为2:1,质量比为1:8.
分析 根据电解水生成气体是“负氢正氧”,且氧气与氢气的体积比是1:2,结合图示所示的气体体积进行解题即可.
解答 解:(1)根据电解水实验正极生成的气体是氧气,负极生成的气体是氢气,且二者的体积比为1:2,有图中可知A管气体体积大为氢气,B管气体体积小为氧气;
(2)B试管内的气体体积较少,所以是氧气,氧气具有助燃性,所以检验B试管内气体的方法是用带火星的木条检验,观察木条是否复燃;
(3)根据电解水实验正极生成的气体是氧气,负极生成的气体是氢气,且二者的体积比为1:2,所以在电解水实验时,甲试管与乙试管内气体的体积比为:2:1,质量比为:1:8..
故答案为:(1)氢,氧;
(2)用带火星的木条检验,观察木条是否复燃;
(3)2:1,1:8.
点评 要熟记正氧负氢,氢二氧一,电解水实验得到的结论有:水是由氢元素和氧元素组成等,以上这些常是解决此类题的关键.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
6.下列说法不符合事实的是( )
| A. | 钢铁生锈是缓慢氧化 | |
| B. | 铁锈的主要成分是四氧化三铁 | |
| C. | 铁在氧气中燃烧生成四氧化三铁 | |
| D. | 及时擦干被雨水淋湿的自行车可防止自行车生锈 |
3.下列不属于大气污染物的是( )
| A. | SO2 | B. | NO2 | C. | 可吸入颗粒物 | D. | CO2 |
10.有关专家提出了“以废治废”的治理污染新思路,并且起到了一定的成效.如冶炼钢铁时,为减少煤中硫燃烧生成的二氧化硫所造成的污染,一般是在煤燃烧时添加生石灰或石灰石进行固硫(主要是利用氧化钙与二氧化硫反应生成亚硫酸钙). 根据这一原理,有人将造纸厂回收的碱白泥(主要成份:CaCO3和NaOH)掺进煤中进行固硫.用碱白泥固硫时,下列说法不正确的是( )
①S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
②CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
③CaCO3+2NaOH═Na2CO3+Ca(OH)2
④SO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSO3
⑤SO2+2NaOH═Na2SO3+H2O.
①S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
②CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
③CaCO3+2NaOH═Na2CO3+Ca(OH)2
④SO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSO3
⑤SO2+2NaOH═Na2SO3+H2O.
| A. | 这些反应都属于基本反应 | |
| B. | 生成物都是含氧化合物 | |
| C. | S在反应①中被氧化 | |
| D. | 上述所写的化学反应能够发生的是①②④⑤ |
7.下列图象与所属实验事实相符的是( )
| A. | 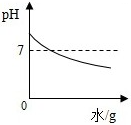 稀释NaOH溶液 | B. |  镁在空气中燃烧 | ||
| C. | 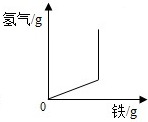 铁加入稀盐酸中 | D. | 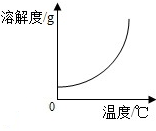 氧气的溶解度 |
4.下列物质放入水中,能形成溶液的是( )
| A. | 豆油 | B. | 面粉 | C. | 汽油 | D. | 白糖 |
5.在一密闭容器中充满空气,经测定其中氮气的体积为100mL,则其中氧气的体积约为( )
| A. | 20mL | B. | 35mL | C. | 40mL | D. | 25mL |