题目内容
4.图是验证质量守恒定律的实验,请问这一装置是否能验证质量守恒定律,并写出此装置的化学方程式.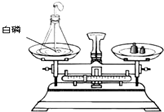
分析 本题考查的是质量守恒定律,其内容是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和如果用的药品生成的是气体、或有气体加入或与空气中的其它成分反应,就必须用密闭的容器进行分析.
解答 解:白磷和氧气反应生成五氧化二磷,反应物中有气体参加,需要在密闭容器中发生反应,气球可以起到缓冲作用,防止气体受热膨胀,将橡胶塞涨开,所以能验证质量守恒定律,化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故答案为:能验证质量守恒定律,4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
点评 本考点是有关质量守恒定律的实验探究,有关质量守恒定律的考题在中考中经常出现,要抓住要点:五个一定不变,一个一定变.还要注意药品的选择和装置的选择.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列化学变化中吸收热量的是( )
| A. | 红磷在氧气中的燃烧 | B. | 高温煅烧石灰石 | ||
| C. | 镁条和稀盐酸的反应 | D. | 石灰石与水反应 |
15.下列金属材料不属于合金的是( )
| A. | 青铜 | B. | 生铁 | C. | 紫铜 | D. | 焊锡 |
 水是重要的自然资源.
水是重要的自然资源.