题目内容
16.实验室里要制取并收集一瓶干燥纯净的CO2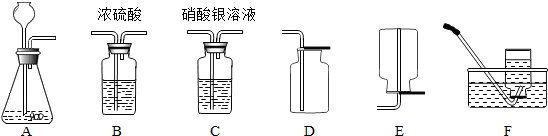
应选工艺装置是A→C→B→D,装置A中盛放的药品为石灰石与稀盐酸,发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 从稀盐酸与碳酸钙反应制取二氧化碳,硝酸银溶液吸收挥发出来的氯化氢气体、浓硫酸可以吸收二氧化碳中的水蒸气,并不与二氧化碳反应,二氧化碳能溶于水且密度比空气大,据此选择收集装置去分析.
解答 解:装置A适用于“固+液 常温型”制取气体,故A装置中的可以通过稀盐酸与碳酸钙反应来制取二氧化碳.盐酸易挥发,所以装置A与盛有吸收氯化氢气体的硝酸银溶液(除去二氧化碳气体中混有氯化氢气体)的装置C连接,然后制取的气体通过盛有浓硫酸(浓硫酸具有吸水性,可做干燥剂)的B装置,可以得到干燥的二氧化碳气体;因为二氧化碳的溶于水且密度比空气大,所以可以采取向上排空气法收集,二氧化碳能溶于水,所以不能用排水法收集.
故答案为:C B D 石灰石与稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题考查实验室制取二氧化碳的装置的选取、方程式的书写、以及药品的选取原则,同学们一定要熟悉常见气体的性质,同时要注意收集干燥的气体时,要在最后一步进行干燥.

练习册系列答案
相关题目
6.保持氧气化学性质的基本粒子是( )
| A. | 氧分子 | B. | 氧原子 | C. | 氧元素 | D. | 电子 |
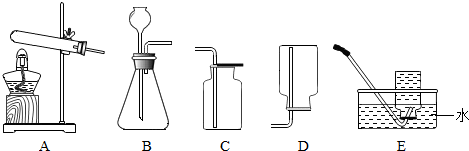
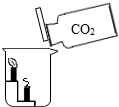 如图所示,将CO2沿烧杯内壁倾倒烧杯中,可看到什么现象?这说明CO2具有哪些性质?
如图所示,将CO2沿烧杯内壁倾倒烧杯中,可看到什么现象?这说明CO2具有哪些性质?