题目内容
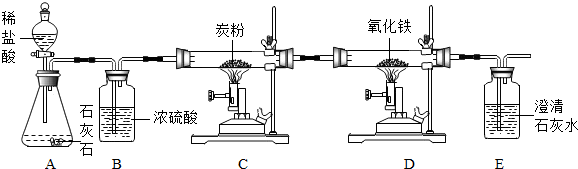
看图回答下列问题:
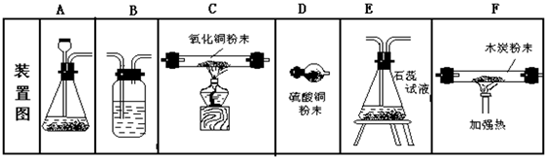
(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色.判断:①A中产生的气体是
②B中用于干燥气体的液体是
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的一种装置的编号.
①写出实验室制CO2的化学方程式
②除去混合气体中的CO2,应通入(填物质的化学式)

(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色.判断:①A中产生的气体是
氢气(H2)
氢气(H2)
.C中的氧化铜由黑色变为红
黑色变为红
色(填颜色的变化),反应前后(用元素符号填充)H、Cu
H、Cu
元素的化合价发生了变化.②B中用于干燥气体的液体是
浓硫酸
浓硫酸
(填物质名称).(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的一种装置的编号.
| 实验 要求 |
制CO2 | 证明CO2与H2O化合 | CO2→CO | CO还原性 | 除去混和气体的水 |
| 装置 编号 |
A A |
E E |
F F |
C C |
B B |
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.②除去混合气体中的CO2,应通入(填物质的化学式)
NaOH
NaOH
溶液.分析:(1)硫酸铜遇水变蓝分析产生气体是氢气,根据化学方程式及化合式分析化合价的升降,浓硫酸具有吸水性.
(2)根据发生装置及验证气体的性质实验进行选择装置,根据化学方程式书写原则书写方程式.
(2)根据发生装置及验证气体的性质实验进行选择装置,根据化学方程式书写原则书写方程式.
解答:解:(1)①按A、B、C、D依次组装进行实验后D装置中硫酸铜粉末由白色变为蓝色.说明气体与氧化铜反应生成水,因此A中产生的气体是氢气,氢气还原氧化铜生成铜和水,因此C中氧化铜由黑色变为红色,化学方程式为:H2+CuO
Cu+H2O,由化学方程式可以看出,氢元素化合价由0价升高为+1价,铜元素由+2价降低为0价.
②浓硫酸具有吸水性,可用作干燥剂,因此B中用于干燥气体的液体是 浓硫酸
(2)实验室用大理石和稀盐酸制二氧化碳,大理石是块状固体,稀盐酸是液体,应选择固液常温型装置,故选A;二氧化碳与水化合生成碳酸,能使紫色石蕊试液变红色,因此选E;二氧化碳与碳反应生成一氧化碳,故选F,一氧化碳还原金属氧化物表现出还原性,故选C;除去混合气体中的水蒸气可用浓硫酸,故选B
①实验室制CO2的化学方程式 CaCO3+2HCl═CaCl2+H2O+CO2↑.
②二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,因此除去混合气体中的CO2,应通入 NaOH溶液.
故答案为:(1)氢气(H2). 黑色变为红 H、Cu②浓硫酸
(2)
①CaCO3+2HCl═CaCl2+H2O+CO2↑.
②NaOH
| ||
②浓硫酸具有吸水性,可用作干燥剂,因此B中用于干燥气体的液体是 浓硫酸
(2)实验室用大理石和稀盐酸制二氧化碳,大理石是块状固体,稀盐酸是液体,应选择固液常温型装置,故选A;二氧化碳与水化合生成碳酸,能使紫色石蕊试液变红色,因此选E;二氧化碳与碳反应生成一氧化碳,故选F,一氧化碳还原金属氧化物表现出还原性,故选C;除去混合气体中的水蒸气可用浓硫酸,故选B
①实验室制CO2的化学方程式 CaCO3+2HCl═CaCl2+H2O+CO2↑.
②二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,因此除去混合气体中的CO2,应通入 NaOH溶液.
故答案为:(1)氢气(H2). 黑色变为红 H、Cu②浓硫酸
(2)
| 除去混和气体中的水 | |||||
| A | E | F | C | B |
②NaOH
点评:硫酸铜遇水变蓝,浓硫酸具有吸水性,是一种液体干燥剂;明确气体的制取和性质验证实验是解答本题关键.

练习册系列答案
相关题目

 (2012?岳阳二模)如图是甲、乙、丙三种固体物质的溶解度曲线.看图回答下列问题:
(2012?岳阳二模)如图是甲、乙、丙三种固体物质的溶解度曲线.看图回答下列问题: