题目内容
18.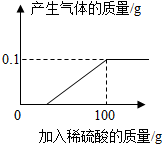 硫酸锌片在医药方面可用于治疗食欲不振、发育不良等症状,实验室可用锌和稀硫酸反应制得.学校化学兴趣小组的同学取一块表面严重氧化的锌片7.3g(不含其它杂质),剪碎,向其中慢慢滴加9.8%的稀硫酸,至恰好完全反应时,用去稀硫酸100g,并绘出如图所示的图象.
硫酸锌片在医药方面可用于治疗食欲不振、发育不良等症状,实验室可用锌和稀硫酸反应制得.学校化学兴趣小组的同学取一块表面严重氧化的锌片7.3g(不含其它杂质),剪碎,向其中慢慢滴加9.8%的稀硫酸,至恰好完全反应时,用去稀硫酸100g,并绘出如图所示的图象.(1)小组同学在老师的指导下,配制200g 9.8%的稀硫酸.
①用98%的浓硫酸配制200g 9.8%的稀硫酸,需加水180gg.
②将配制好的稀硫酸转移到试剂瓶中,贴上标签,标签上必须注明的是BC(填序号).
A.200g B.9.8% C.稀硫酸
③下列操作中的AC(填序号),可能会导致配制的溶液的溶质的质量分数低于9.8%.
A.量取浓硫酸后,置于空气中时间过长
B.量水时,俯视量筒刻度
C.配制前将烧杯用水冲洗干净,没有擦干
(2)生成0.1g氢气消耗的稀硫酸的质量是多少?(请写出完整的计算过程)
分析 (1)①根据溶液稀释前后溶质质量相等进行分析;
②根据试剂瓶上需要注明药品的名称和溶质质量分数进行分析;
③根据导致配制的溶液的溶质的质量分数低于9.8%的可能原因是溶质少了或溶剂多了进行分析;
(2)根据锌和硫酸反应生成硫酸锌和氢气,依据氢气的质量进行计算;
解答 解:(1)①用98%的浓硫酸配制200g9.8%的稀硫酸,需加水的质量为:200g-$\frac{200g×9.8%}{98%}$=180g;
②试剂瓶上需要注明药品的名称和溶质质量分数,故选:BC;
③导致配制的溶液的溶质的质量分数低于9.8%的可能原因是溶质少了或溶剂多了,
A、量取浓硫酸后,置于空气中时间过长,导致浓硫酸的质量减少了,所以溶质质量分数偏低,故A正确;
B、量水时,俯视量筒刻度,水的体积少了,导致溶质质量分数偏大,故B错误
C、配制前将烧杯用水冲洗干净,没有擦干,导致溶剂的质量多了,所以溶质质量分数偏低,故C正确,
故选:AC;
(2)设生成0.1g氢气消耗的稀硫酸的质量是x
Zn+H2SO4=ZnSO4+H2↑
98 2
x×9.8% 0.1g
$\frac{98}{x×9.8%}=\frac{2}{0.1g}$
x=50g
故答案为:(1)①180g;
②BC;
③AC;
(2)50g;
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.在一定条件下,下列物质间的转化能一步实现的是( )
①Fe→Fe3O4 ②S→SO3 ③CuCl2→Cu ④Na2O→NaOH.
①Fe→Fe3O4 ②S→SO3 ③CuCl2→Cu ④Na2O→NaOH.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
9.逻辑推理是学习化学常用的思维方法,下列推理正确的是( )
| A. | 物质的分子结构不同则化学性质不同,所以氧气和臭氧(O3)的化学性质不同 | |
| B. | 由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成 | |
| C. | 氧、硫、氯原子最外层电子数均多于4个,所以非金属元素原子最外层电子数都多于4个 | |
| D. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 |
6.下列变化中,属于化学变化的是( )
| A. | 香水挥发 | B. | 牛奶变酸 | C. | 车胎爆炸 | D. | 石油分馏 |
13.生产“达菲”的主要原料是莽草酸(C7H10O5),下列关于莽草酸的说法正确的是( )
| A. | 莽草酸中氢元素的质量分数最高 | |
| B. | 莽草酸中碳、氢、氧的质量比是7:10:5 | |
| C. | 莽草酸是由22个原子构成的化合物 | |
| D. | 莽草酸由碳、氢、氧三种元素组成 |
3.下列实验操作正确的是( )
| A. |  取用液体 | B. | 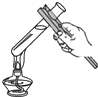 加热液体 | C. |  稀释浓硫酸 | D. |  蒸发食盐水 |
10.如图是初中化学中几个重要实验,下列叙述不正确的是( )
| A. | 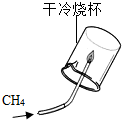 烧杯内产生水雾,说明甲烷燃烧的产物中一定有水 | |
| B. | 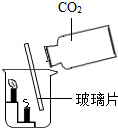 下层的蜡烛先熄灭,说明二氧化碳不支持燃烧本身不燃烧且密度比空气大 | |
| C. | 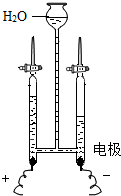 正极与负极的体积比为1:2,说明水中氢元素和氧元素的质量比为1:2 | |
| D. |  铜片上的白磷燃烧,水中的白磷不燃烧说明物质燃烧必须与充足的氧气接触 |
7.分类是化学学习过程中常用的方法,下列分类中不正确的是( )
| A. | 氧化物:生石灰、铁锈和干冰 | |
| B. | 合成材料:合成纤维、塑料和合成橡胶 | |
| C. | 单质:金刚石、液氧和铜粉 | |
| D. | 复合肥:磷酸二氢钾、磷酸氢二铵、硝酸钾 |