题目内容
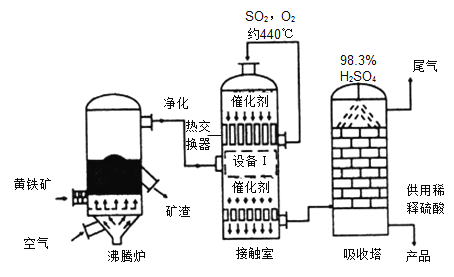
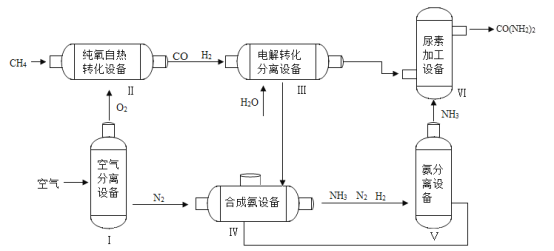
【题目】氢氧化钙 [Ca(OH)2] 是重要的建筑材料,工业上常以石灰石(主要成分为CaCO3)为原料生产氢氧化钙,主要流程如下:

(1)氢氧化钙[Ca(OH)2]的组成元素中,属于金属元素的是_______________。
(2)粉碎石灰石的目的是_____________。
(3)煅烧炉中,发生的反应为CaCO3![]() CaO + CO2↑,此反应属于基本反应类型中________反应。
CaO + CO2↑,此反应属于基本反应类型中________反应。
(4)消化池中发生的反应为CaO +H2O = Ca(OH)2 ,若56t CaO参加反应,可产生的Ca(OH)2 质量为________t。
【答案】钙元素(Ca) 增大反应物的受热面积,使反应更充分 分解 74
【解析】
(1)氢氧化钙[Ca(OH)2]的组成元素中,属于金属元素的是:钙元素。
(2)粉碎石灰石的目的是:增大反应物的受热面积,使反应更充分;
(3)该反应中反应物为一种,生成物为两种,属于分解反应;
(4)设生成氢氧化钙的质量为x:
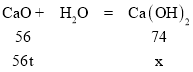
![]()
x=74t

 阅读快车系列答案
阅读快车系列答案【题目】兴趣小组在探究物质燃烧条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿熄灭了。它为什么会熄灭呢?
(提出猜想)甲同学说:蜡烛燃烧耗尽了瓶内的氧气,所以蜡烛熄灭。乙同学说:蜡烛燃烧后瓶内可能还有少量氧气,但有CO2浓度过高导致蜡烛熄灭。
(实验验证)
实验步骤 | 实验现象 | 实验分析 | 实验结论 |
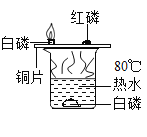
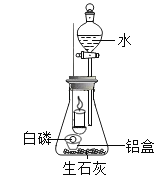
(1)取一小块白磷(着火点为40℃),放在一铝箔制的小盒中,然后放入装有生石灰的锥形瓶内(如图),点燃蜡烛。 | 燃烧的蜡烛一会儿就熄灭了。 | 白磷燃烧需满足的条件: ①温度要达到着火点; ②_____。 | _____同学猜想正确。 |
(2)待冷却后,打开分液漏斗活塞,向锥形瓶中注入少量水,立即关闭活塞。 | 铝盒中的白磷燃烧,放出热量,产生_____。 |
(实验反思)
①在实验中,生石灰的主要作用有两个a._____,b._____。
②实验结束后,同学们对集气瓶底部的含钙固体又产生了兴趣并设计了如下实验:
实验过程 | 现象 | 结论 |
实验1:取样,_____ | 放出大量热 | 该固体中含有_____ |
实验2:取样,滴加无色酚酞 | _____ | 该固体中含有氢氧化钙 |
实验3:取样,滴加足量_____ | 有气泡冒出 | 该固体中含有碳酸钙 |
经小组讨论发现,实验_____(填序号)的结论错误,理由是_____。
【题目】有限的元素可组成种类繁多的物质,依据表中的元素回答下列问题。
元素名称 | 氢 | 碳 | 氧 | 钙 | 铁 |
元素符号 | H | C | O | Ca | Fe |
(1)若某物质是相对分子质量最小的氧化物,该物质的化学式是_____。
(2)若某可燃性气体在氧气中燃烧,能生成两种氧化物,该气体一定含有的元素是_____。
(3)若某元素组成的单质及其氧化物,均能和X发生化合反应生成同一种物质。任写一个相关反应的化学方程式_____。
(4)甲~己六种物质的转化关系如下图所示。已知甲能使澄清石灰水变浑浊;己是无色溶液,能在某种黑色固体物质催化下,生成可供给呼吸的气体。(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化)下列说法正确的是_____(填序号)。

a.丁和己一定含有相同元素 b.乙生成甲和丁一定需要点燃
c.戊转化成甲可能发生置换反应 d.上述反应一定都有气体生成