题目内容
15. 老师用如图所示装置为同学们做如下实验:A装置集气瓶中装有体积比约为1:1的氮气和气体a的混合气体,注射器中装有足量的无色溶液b;B装置中盛有少量紫色石蕊溶液;C装置中盛有适量生锈的铁钉;D装置中盛有足量的稀硫酸.
老师用如图所示装置为同学们做如下实验:A装置集气瓶中装有体积比约为1:1的氮气和气体a的混合气体,注射器中装有足量的无色溶液b;B装置中盛有少量紫色石蕊溶液;C装置中盛有适量生锈的铁钉;D装置中盛有足量的稀硫酸.(1)关闭活塞K1、K2,将注射器中的溶液b挤入瓶中,打开活塞K1,看到B中溶液进入A中后溶液变为蓝色,B中长导管脱离液面.请回答:
①若a气体是二氧化碳,则b是NaOH 溶液(填化学式).
②若b是水,则气体a可能是NH3 (填化学式).
(2)保持K1开启状态,并打开K2,一段时间后关闭K2,整个过程中,观察到D中的现象是AB (填编号,共2分);写出C装置中反应的化学方程式是Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,Fe+H2SO4=FeSO4+H2↑.
A.广口瓶内液面下降 B.长颈漏斗内液面上升 C.长颈漏斗下端有气泡.
分析 (1)根据B中溶液进入A中后溶液变为蓝色,说明气体与溶液b反应造成气压降低,且生成了碱性物质进行分析;
(2)由A装置内气压较小,导致B装置内气压也减小,在外界大气压的作用下再分析题目.
解答 解:(1)由题意可知,B中溶液进入A中后溶液变为蓝色,说明气体与溶液b反应造成气压降低,且生成了碱性物质;
①若a气体是二氧化碳,则b必须是能与二氧化碳反应的物质,故可能是氢氧化钠溶液,化学式是:NaOH;
②若b是水,则气体a应易溶于水,且溶于水后呈碱性,因此a可能是氨气,化学式是:NH3;.
(2)由于A装置中的气体与溶液反应,造成气压减小,B中液体进入A,C中气体进入B,故D中的稀硫酸进入装置C,然后与生锈的铁钉发生反应,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑,由于氢气的生成,气压升高,故观察到D中的现象是:广口瓶内液面下降,长颈漏斗中的液面上升.
故答案为:(1)①NaOH;②NH3;(2)AB;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe+H2SO4=FeSO4+H2↑.
点评 通过回答本题可知有些题目需要结合物理知识来回答,并且利用外界大气压与瓶内的压力差来做题

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
6.下列实验现象描述不正确的是( )
| A. | 氢氧化钠固体放入水中,液体温度升高 | |
| B. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 电解水时正极产生的气体体积比负极产生的气体体积多 | |
| D. | 高温条件下木炭还原氧化铜:黑色固体逐渐变成红色 |
7.对于下列化学用语,有关说法正确的是( )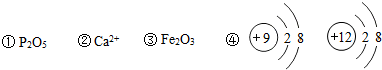
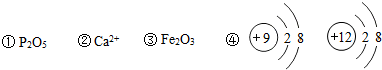
| A. | ①可表示五氧化二磷分子是由磷和氧两种元素组成 | |
| B. | ②和④均表示阳离子 | |
| C. | ③Fe2O3属于金属氧化物能与稀盐酸反应 | |
| D. | ④和⑤对应的元素都在元素周期表第二周期 |
3.下列属于物质物理性质的是( )
| A. | CO的毒性 | B. | 酒精的可燃性 | ||
| C. | 铜是紫红色的固体 | D. | 浓硫酸的腐蚀性 |
4.能说明酒精溶液是混合物的( )
| A. | 溶液有特殊的气味 | B. | 溶液在空气中能燃烧 | ||
| C. | 溶液是无色的 | D. | 溶液中含有两种分子 |