题目内容
金属M与AgNO3溶液发生反应:M+2AgNO3=M(NO3)2+2Ag,下列说法正确的是( )
|
| A. | M可能是铝 |
|
| B. | Ag的金属活动性比M强 |
|
| C. | 反应前后M的化合价发生了改变 |
|
| D. | 在金属活动性顺序里,M一定排在氢前 |
考点:
金属的化学性质.
专题:
金属与金属材料.
分析:
根据金属活动性顺序的应用分析推断.根据题意,金属M能与硝酸银反应置换出银,说明M的活动性比银强;由生成了M(NO3)2可知,M在化合物中的化合价为+2价;结合选项进行分析.
解答:
解:A、由M与硝酸银溶液反应的生成了M(NO3)2,则M在化合物中的化合价为+2价,铝与硝酸银溶液反应生成了硝酸铝,铝为+3价,故该金属不可能是铝,故说法错误;
B、由于金属M能与硝酸银反应置换出银,说明M的金属活动性比银强,故说法错误;
C、反应前M为单质,元素的化合价为0,反应后表现为+2,故说法正确;
D、由于金属M能与硝酸银反应置换出银,说明M的金属活动性比银强,但M不一定排在氢前,故说法错误;
故选项为:C.
点评:
本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行分析:金属单质能置换出盐中的金属,说明组成单质的金属元素的活动性比盐中金属元素的活动性强.

下列说法不正确的是( )
|
| A. | 单质铁能从硫酸铜溶液中把铜置换出来 |
|
| B. | 能使无色酚酞溶液变红的物质,一定是碱溶液 |
|
| C. | 碘是人体必须的微量元素,缺碘会引起甲状腺肿大 |
|
| D. | 燃烧必须同时满足两个条件:可燃物与氧气接触、可燃物的温度达到着火点 |
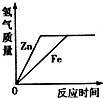
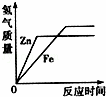
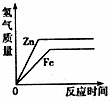
向等质量的锌粉和铁粉中分别加入足量稀硫酸,下列图象描述正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
下列有关溶液的说法中,正确的是( )
|
| A. | 溶液都是无色、透明的 |
|
| B. | 均一、稳定的液体都是溶液 |
|
| C. | 硝酸铵溶于水,使溶液的温度降低 |
|
| D. | 溶质都以分子形式溶解在溶剂里 |