题目内容
在高温条件下,让炭粉和氧化铜组成的混合物18g充分反应,其中有一种物质已完全参加反应,反应结束后冷却到室温,称量剩余物的质量为13.6g,则通过计算回答:
①剩余物中铜的质量分数(计算结果精确到0.1%);
②剩余物中除了Cu还有什么物质?,应有多少克?
①剩余物中铜的质量分数(计算结果精确到0.1%);
②剩余物中除了Cu还有什么物质?,应有多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:因为碳完全反应所以反应前后固体的质量之差即为碳与氧化铜反应生成的二氧化碳质量,利用该值即可依据方程式求出生成物中铜的质量.
解答:解:①依据质量守恒定律可知生成CO2的质量为18g-13.6g=4.4g;
设生成铜的质量为x,参加反应的氧化铜的质量为y,参加反应的碳的质量为z.
C+2CuO
CO2↑+2Cu
12 160 44 128
z y 4.4g x
=
=
=
x=12.8g y=16g z=1.2g
剩余物中铜的质量分数:
×100%=94.1%;
②剩余物中除了Cu还可能有碳或氧化铜,质量为:18g-16g-1.2g=0.8g;
答:①剩余物中铜的质量分数94.1%;
②剩余物中除了Cu还可能有碳或氧化铜,质量为0.8g.
设生成铜的质量为x,参加反应的氧化铜的质量为y,参加反应的碳的质量为z.
C+2CuO
| ||
12 160 44 128
z y 4.4g x
| 44 |
| 4.4g |
| 128 |
| x |
| 160 |
| y |
| 44 |
| 4.4g |
| 12 |
| z |
| 44 |
| 4.4g |
x=12.8g y=16g z=1.2g
剩余物中铜的质量分数:
| 12.8g |
| 13.6g |
②剩余物中除了Cu还可能有碳或氧化铜,质量为:18g-16g-1.2g=0.8g;
答:①剩余物中铜的质量分数94.1%;
②剩余物中除了Cu还可能有碳或氧化铜,质量为0.8g.
点评:此题是对化学方程式计算的考查题,解题的关键是掌握固体的质量变化即是生成的二氧化碳的质量.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
能把稀盐酸、Ca(OH)2、NaCl三种溶液区分开的是( )
| A、石蕊 | B、氯化钙 |
| C、酚酞 | D、二氧化碳 |
下列实验操作中,正确的是( )
A、 读液体体积 |
B、 倾倒液体 |
C、 过滤 |
D、 浓硫酸的稀释 |
今年元月份我国多个城市多次遭遇雾霾天气,空气污染指数纷纷爆表,其中PM2.5是形成雾霾天气的最大元凶.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物,对人体健康影响很大,主要来源于直接排放的工业污染物和汽车尾气等.下列说法正确的是( )
| A、燃放烟花爆竹不会造成大气污染 |
| B、吸入PM10的颗粒物对人体健康没有危害 |
| C、为了减小PM2.5对环境的影响,禁止家庭使用私家车 |
| D、香烟烟雾颗粒的直径大多在0.1至1.0微米,提倡不吸或少吸烟 |
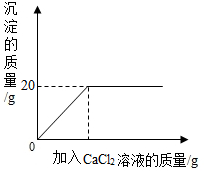 将一定质量的碳酸钠粉末溶于200g水中配制成溶液,取
将一定质量的碳酸钠粉末溶于200g水中配制成溶液,取 小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求:
小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求: 如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题: