题目内容
10.将25g二氧化锰与氯酸钾的混合物共热到质量不减少为止,称得固体残渣质量为15.4g.求:(1)生成氧气多少克?
(2)原先混合物中氯酸钾的质量是多少克?
分析 氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,由质量守恒定律,固体混合物减少的质量即为产生氧气的质量,据此由氧气的质量结合反应的化学方程式进行分析解答即可.
解答 解:(1)生成氧气的质量为25g-15.4g=9.6g.
(2)设参加反应的氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{x}$=$\frac{96}{9.6g}$
x=24.5g
答:(1)生成氧气9.6g;(2)原先混合物中氯酸钾的质量是24.5g.
点评 本题难度不大,掌握利用化学方程式的计算、固体混合物减少的质量即为产生氧气的质量是正确解答本题的关键.

练习册系列答案
相关题目
19.我们学化学、用化学、爱化学,让化学知识服务于人类.下列叙述正确的是( )
| A. | 用甲醛的水溶液浸泡海产品保鲜 | |
| B. | 尿素(CO(NH2)2)、HNO3、NH4HCO3中都含氮元素,可用作氮肥 | |
| C. | 不锈钢、玻璃钢都是金属材料,可以作医疗手术器械 | |
| D. | 洗洁精含有乳化剂,可以除去油污 |
20.下列鉴别方法错误的是( )
| 待鉴别的物质 | 鉴别方法 | |
| A | 腈纶和羊毛纤维 | 燃烧,闻燃烧产生的气味 |
| B | 食盐溶液和盐酸 | 滴加无色酚酞试液,观察溶液颜色的变化 |
| C | 氯化铵和尿素[CO(NH2)2] | 与熟石灰混合后一起研磨,闻气味 |
| D | CO2和CO | 通入澄清石灰水中,观察溶液是否变浑浊 |
| A. | A | B. | B | C. | D |
2.小科在实验室发现一瓶浑浊的石灰水,瓶壁上有一层白膜.关于这瓶石灰水,下列说法不正确的是( )
| A. | 石灰水是混合物 | |
| B. | 检验二氧化碳不宜用该瓶石灰水 | |
| C. | 瓶壁上白膜可能是碳酸钙 | |
| D. | 澄清的石灰水变浑浊后溶液质量增加 |
20.下列反应属于中和反应的是( )
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$ SO2 | B. | 2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$ CO2↑+2Cu | D. | Al(OH)3+3HCl═AlCl3+3H2O |
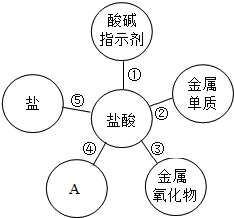 归纳是重要的学习方法,小红在复习盐酸的性质是,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是重要的学习方法,小红在复习盐酸的性质是,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).