题目内容
金属袁术形成的化合物,依据物质的组成常分为氧化物、碱和盐.

(1)在元素周期表中,镁元素的信息如图1所示,镁原子的结构示意图为 ,镁原子在化学变化中容易失去 个电子.
(2)某酸(HR)与盐酸具有相似的化学性质,写出HR与镁反应的化学方程式 .
(3)甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱.它们之间的转化关系如图2(部分反应物和产物已略去,“→”表示吴志坚存在转化关系).请回答:
①甲的俗名为 ;
②丙→甲的化学反应方程式为 ;
③乙→丁的化学反应方程式为 (任写一个).
| 元素周期表的特点及其应用;酸的化学性质;物质的鉴别、推断;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 框图型推断题;化学用语和质量守恒定律. |
| 分析: | (1)结合镁元素的原子序数来书写原子结构示意图,根据其最外层电子数来分析得失电子情 (2)根据酸的通性来分析解答; (3)根据题干信息和物质间的转化关系来分析解答. |
| 解答: | 解:(1)由元素周期表中的信息可知,镁的原子序数为12,则其核内质子数和核外电子数均为12,核外电子排布为:2、8、2结构,最外层有2个电子,在化学变化中易失去2个电子; (2)HR与镁发生置换反应生成盐和氢气; (3)因为四种物质中均含钙元素,则氧化物就是氧化钙,碱就是氢氧化钙,由物质间的转化关系可知,丙是碳酸钙,丁是氯化钙或硫酸钙或硝酸钙;甲是氧化钙,乙是氢氧化钙. 故答案为:(1)
(2)Mg+2HR=MgR2+H2↑; (3)①生石灰; ②CaCO3 ③Ca(OH)2+2HCl=CaCl2+2H2O(其他合理答案也可). |
| 点评: | 本题考查的知识点较多,但是难度不大. |

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案某同学设计了以下三个实验,要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是( )
|
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
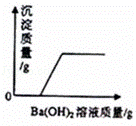
某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
|
| A. | HCl和H2SO4一定存在 |
|
| B. | NaOH、H2SO4和MgCl2一定不存在 |
|
| C. | HCl和MgCl2一定存在 |
|
| D. | HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在 |
某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
| R | O2 | CO2[来源:Z§xx§k.Com] | H2O | |
| 反应前质量(g) | 51 | 96 | 0 | 0 |
| 反应后质量(g) | x | 0 | 88 | 54 |
下列说法中不正确的是( )
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
 况;
况;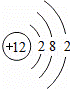 ;2;
;2; CaO+CO2↑;
CaO+CO2↑;

