题目内容
1.如图1是实验室制取气体的部分装置,请回答下列问题: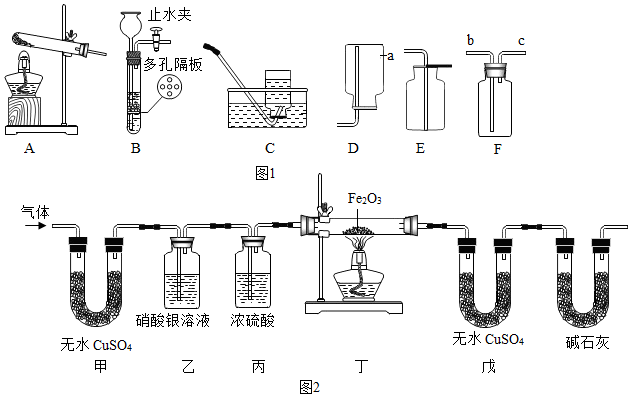
(1)写出仪器a的名称集气瓶.
(2)氢气是最理想的燃料.通常状况下,氢气密度比空气小,难溶于水.欣悦同学用锌粒与盐酸反应制取氢气,选择的装置组合是BC或BD(填字母),该发生装置的优点是可以使反应随时发生,随时停止,若用F装置排空气法收集氢气,气体应从c端进入(填b或c).
【提出问题】①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
【设计实验方案】欣悦同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收).
【实验现象和结论】
| 实验现象 | 实验结论 |
| 甲装置中的白色固体变成蓝色 | 气体中有H2O |
| 乙装置中产生白色沉淀 | 气体中有HCl |
| 丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应 丁装置中玻璃管内反应的化学方程式 为3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O |
①根据丁装置中实验现象,说明氢气具有还原性.
②丁装置加热前通入H2的目的是排净装置内的空气,以防加热时发生爆炸.
分析 (1)熟记仪器的名称;
(2)根据反应物的状态与反应的条件来确定制取装置,根据氢气的密度来确定收集的方法;
【实验现象和结论】根据盐酸的化学性质来分析;结合化学反应的原理以及化学方程式的写法来分析;
【交流总结】①根据实验现象来分析氢气的化学性质;
②根据氢气具有可燃性来分析.
解答 解:(1)仪器a是集气瓶;故填:集气瓶;
(2)用锌粒与盐酸反应制取氢气属于固液常温型,所以选择装置B,该装置可以使反应随时发生,随时停止;氢气难溶于水,可用排水法收集,氢气的密度比空气小,可用向上排空气法来收集,用装置F收集氢气时,氢气从短管进入;故填:BC或BD;可以使反应随时发生,随时停止;c;
【实验现象和结论】若气体中含有HCl,氯化氢溶于水则为盐酸,盐酸能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,也就是乙装置中产生了白色沉淀;故填:白色沉淀;
丁装置中玻璃管内红色粉末变成黑色说明氧化铁转化为了铁;戊装置中白色固体变成蓝色说明生成了水,也就是在加热的条件下,氢气与氧化铁反应生成铁和水;故填:3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O;
【交流总结】①根据丁装置中实验现象可知,氢气能够夺取氧化铁中的氧元素,将其转化为铁,这说明了氢气具有还原性;故填:还原;
②氢气具有可燃性,丁装置加热前通入H2的目的是排净装置内的空气,以防加热时发生爆炸;故填:排净装置内的空气,以防加热时发生爆炸.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
相关题目
11.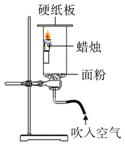 如图往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭.下列说法正确的是( )
如图往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭.下列说法正确的是( )
 如图往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭.下列说法正确的是( )
如图往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭.下列说法正确的是( )| A. | 在有限的作业空间,可燃性粉尘遇明火一定会发生燃爆 | |
| B. | 蜡烛熄灭是因为蜡烛的着火点改变了 | |
| C. | 发生燃爆后体系的温度升高,氧气耗尽蜡烛熄灭 | |
| D. | 实验用的容器可以用废旧矿泉水瓶,也可以用玻璃瓶 |
12.如图是硝酸钾的溶解度曲线,某同学在20℃时进行了如图2所示的实验,得到相应的溶液①-⑤,下列说法正确的是( )
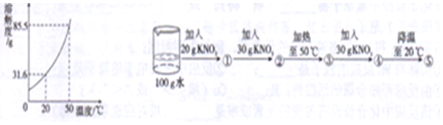

| A. | 保持温度不变,若在④中加入4.5gKNO3固体可得到饱和溶液 | |
| B. | ②③⑤中溶质的质量分数相等 | |
| C. | ①③④均为不饱和溶液 | |
| D. | ④→⑤可析出53.9gKNO3晶体 |
9.2017年3月,永嘉县制定了“一河一策”,开展全境剿灭劣五类水行动.下列措施中有利于剿灭劣五类水的是( )
| A. | 任意排放工业污水 | B. | 禁止使用农药和化肥 | ||
| C. | 生活污水经净化处理后再排放 | D. | 抑制水中所有植物生长 |
13.据报道,我国科学家发现一种氦钠化合物(化学式为Na2He),下列说法正确的是( )
| A. | Na2He中Na为+1价,He为-1价 | |
| B. | Na2He中Na、He元素的质量比为2:1 | |
| C. | Na2He中既含金属元素,也含非金属元素 | |
| D. | 稀有气体都很稳定,不与任何物质反应 |
13.2017年3月22日是第二十五届“世界水口”,我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.下列有关水的说法正确的是( )
| A. | 为了保护水资源,禁止使用农药和化肥 | |
| B. | 天然水经过沉降、吸附、杀菌消毒等过程得到的水属于纯净物 | |
| C. | 电解水时,负极得到的气体能燃烧并产生淡蓝色火焰 | |
| D. | 保持水化学性质的最小粒子是氧原子和氢原子 |