题目内容
10.某兴趣小组对物质的性质和成分进行相关探究.(1)常见金属活动性顺序如下,填写相应的元素符号:

某同学用硫酸铜溶液把“把铁刀变成铜刀”,其反应的化学方程式为Fe+CuSO4=Cu+FeSO4.
(2)兴趣小组同学用氧化铜与足量的炭粉利用图甲所示装置进行实验,对生成气体的成分进行探究.

【提出问题】生成的气体中是否含有一氧化碳?
【实验与讨论】
①打开K,缓缓通入干燥的氮气一段时间.
②关闭K,加热至一定温度使之反应,用气囊收集气体样品.
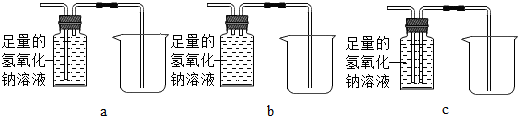
③除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列装置中最为合理的是c.
【实验求证】
将除尽二氧化碳后的气体样品干燥,仍然用图甲所示的装置进行实验,A中的固体应选用氧化铜,B中溶液为澄清石灰水,若A中黑色固体出现了红色,B中澄清石灰水变浑浊,可说明气体样品中含有一氧化碳.
【实验反思】
炭粉还原氧化铜的实验中,若生成的气体中含有一氧化碳,则反应时消耗碳、氧元素的质量比大于(填“大于”、“等于”或“小于”)3:8.
分析 (1)根据金属活动性顺序表的应用分析解答.
(2)【实验与讨论】观察装置的特点,分析除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中的最为合理装置.
【实验求证】根据实验的目的,分析A中应加入的固体、实验的现象等.
【实验反思】根据一氧化碳、二氧化碳中碳、氧元素比分析.
解答 解:(1)由金属的活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au可知,在金属活动顺序表空格内应填入Mg、Ag;铁与硫酸铜溶液反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4;
(2)【实验与讨论】除去气体样品中的二氧化碳,应将气体通入到氢氧化钠溶液中,由于一氧化碳的密度小于水的密度,可通过右边长导管将氢氧化钠排出,将气体收集在集气瓶中,所以,最为合理装置是c;
【实验求证】为了验证生成的气体中是否含有一氧化碳,A中应加入的固体是氧化铜,实验的现象是B中澄清石灰水浑浊,可说明气体样品中含有一氧化碳等.
【实验反思】由于在一氧化碳、二氧化碳中,碳、氧元素的质量比分别是3:4、3:8,所以,炭粉还原氧化铜的实验中,若生成的气体中含有一氧化碳,则反应时消耗碳、氧元素的质量比大于3:8.
故答案为:(1)Mg、Ag,Fe+CuSO4=Cu+FeSO4;
(2)【实验与讨论】c;【实验求证】氧化铜、变浑浊;【实验反思】大于.
点评 解答本题的关键是熟记金属活动性顺序表及其应用、碳和一氧化碳还原氧化铜实验的知识.

练习册系列答案
相关题目
1.在宏观、微观和符号之间建立联系是化学学科的特点.现有A、B、C、D四种物质,其微观示意图见表.
(1)B物质相对分子质量为18
(2)上述物质中属于单质的是D(填物质序号)属于有机物的是CH4(填写化学式)
(3)一个C分子是由两个氧原子和一个碳原子构成的;
(4)写出反应A+D→B+C的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
| 物质 | A | B | C | D | 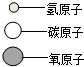 |
| 微观示意图 | 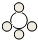 |  | 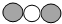 |  |
(2)上述物质中属于单质的是D(填物质序号)属于有机物的是CH4(填写化学式)
(3)一个C分子是由两个氧原子和一个碳原子构成的;
(4)写出反应A+D→B+C的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
5.将下列pH不同的各组溶液混合,所得溶液的pH可能为7的是( )
| A. | pH=9、pH=0 | B. | pH=2、pH=5 | C. | pH=12、pH=7 | D. | pH=5、pH=7 |
15.某气体物质质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量为( )
| A. | 64 | B. | 32 | C. | 96 | D. | 32 |
20.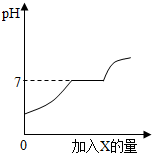 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH 随滴入X的量的变化关系如图所示.则 X 是( )| A. | 稀盐酸 | B. | 澄清石灰水 | C. | 水 | D. | 纯碱溶液 |
 生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.
生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识填空.
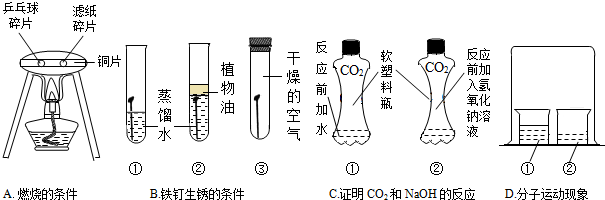
 在对蜡烛及其燃烧进行了探究以后,请你填写下列空格:
在对蜡烛及其燃烧进行了探究以后,请你填写下列空格: