题目内容
8.用化学方程式表示下列反应原理.(1)用氢氧化铝治疗胃酸过多.Al(OH)3+3HCl═AlCl3+3H2O
(2)农业上不能用铁制容器配制农药波尔多液(含硫酸铜)Fe+CuSO4═FeSO4+Cu.
(3)实验室加热固体制取氧气.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(写出一个即可)
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)氢氧化铝能与胃液中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O;
(2)铁和硫酸铜反应生成铜和硫酸亚铁,化学方程式为:Fe+CuSO4═FeSO4+Cu;
(3)高锰酸钾在受热的条件下生成锰酸钾、二氧化锰和氧气,故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
故答案为:(1)Al(OH)3+3HCl═AlCl3+3H2O;(2)Fe+CuSO4═FeSO4+Cu;(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
18.小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体.在反应过程中,溶液的温度也先随之升高,最后下降到室温.于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”.测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有盐酸溶液浓度、反应时溶液的温度.
(2)可以通过比较反应开始到2分钟产生的气体体积实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,其主要影响因素是:温度;当反应进行一段时间后速率又逐渐减慢,其主要影响因素是:浓度.
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
(2)可以通过比较反应开始到2分钟产生的气体体积实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,其主要影响因素是:温度;当反应进行一段时间后速率又逐渐减慢,其主要影响因素是:浓度.
19.金属具有共同的物理性质的是( )
| A. | 熔点高,硬度大 | B. | 有磁性,能被磁体吸附 | ||
| C. | 能导电、导热 | D. | 都是固体 |
16.实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红.他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红.为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了.四位同学依据所学的化学知识,分别对上述酚酞试液变红、红色又消失的原因作了如下猜想:
小明:可能是个偶然现象.
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故.
小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象.他们的方法是:做重复实验.
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是固体氢氧化镁中没有自由移动的OH一离子,不能使酚酞试液变红.
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
(4)对小红的猜想,实验小组的同学设计了多种实验方案进行证明.请你写出其中一种.
小明:可能是个偶然现象.
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故.
小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象.他们的方法是:做重复实验.
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是固体氢氧化镁中没有自由移动的OH一离子,不能使酚酞试液变红.
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
| 实验步骤 | 设计目的 |
| 将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油. | ①隔绝空气证明红色消失与氧气和二氧化碳无关 |
| 实验方法 | 可能观察到的现象 | 相应结果或结论 |
| ①取两支试管,分别加入相同质量的氢氧化镁和相同质量的热水振荡,各滴加数滴酚酞试液.一支保持温度不变,另一支自然冷却. | ② 保持温度不变的红色不消失(或消失),自然冷却的红色消失. | ③红色消失与氢氧化镁的溶解度随温度降低而减小有关(或无关). |
3.发明了“联合制碱法”的科学家是 ( )
| A. |  侯德榜 | B. |  拉瓦锡 | C. |  门捷列夫 | D. |  张青莲 |
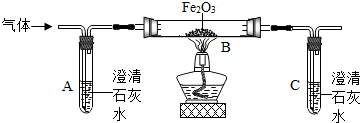
17.某学习小组设计如图实验装置,通入纯净气体后,给黑色固体粉末加热.
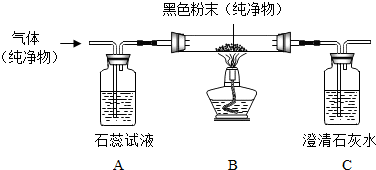
(1)请根据如表中对可能出现的实验现象的描述,推测气体、黑色粉末可能的组合.
(2)若从环保的角度分析,该实验装置可能存有不完善之处.该做怎样的改进在C后加燃着的酒精灯.

(1)请根据如表中对可能出现的实验现象的描述,推测气体、黑色粉末可能的组合.
| 可观察到的实验现象 | 气体的 化学式 | 黑色固体的化学式 | ||
| A中紫色石蕊试液 | C中澄清石灰水 | |||
| ① | 不变色 | 变浑浊 | ||
| ② | 变红色 | 无变化 | ||
 蚊虫叮咬分泌出蚁酸刺激皮肤,某兴趣小组对蚁酸进行如下探究.
蚊虫叮咬分泌出蚁酸刺激皮肤,某兴趣小组对蚁酸进行如下探究.